
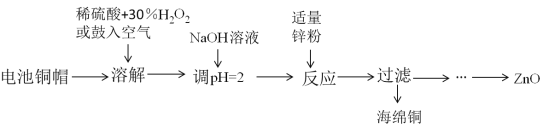
【题目】为研究废旧电池的再利用,实验室利用旧电池的铜帽(主要成分为Zn和Cu)回收Cu并制备ZnO的部分实验过程如图所示。下列叙述错误的是( )
A.“溶解”操作中溶液温度不宜过高
B.铜帽溶解后,将溶液加热至沸腾以除去溶液中过量的氧气或H2O2
C.与锌粉反应的离子可能为Cu2+、H+
D.“过滤”后,将滤液蒸发结晶、过滤、洗涤、干燥后高温灼烧可得纯净的ZnO
【答案】D
【解析】
电池的铜帽(主要成分为Zn和Cu)加入H2SO4和H2O2或鼓入空气,Zn和Cu都转化为离子,调pH至2,可将溶液中的H+中和一部分,加入Zn可将溶液中的Cu置换出来,再过滤得到Cu,溶液中的Zn2+经过处理后最终得到ZnO。
A.由流程图可知,溶解时加入了30%H2O2,H2O2受热易分解,故“溶解”操作中溶液温度不宜过高,A正确;
B.过氧化氢受热易分解,所以可以用加热的方法除去过量的过氧化氢,氧气是气体,在水中的溶解度随温度升高而降低,所以用加热的方法也可以除去氧气,B正确;
C.调节pH后的溶液中含有的阳离子是Zn2+、Cu2+、H+,Cu2+、H+都能与锌粉反应,C正确;
D.滤液中含有硫酸锌和硫酸钠,所以将滤液蒸干、高温灼烧得到氧化锌和硫酸钠,不能得到纯净的氧化锌,D错误;
故选D。


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】有可逆反应Fe(s)+CO2(g)![]() FeO(s)+CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2。则下列说法不正确的是
FeO(s)+CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2。则下列说法不正确的是
A. 该反应的平衡常数表达式为K=c(CO)/c(CO2)
B. 该反应的逆反应是放热反应
C. v正(CO2)=v逆(CO)时该反应达到平衡状态
D. c(CO2):c(CO)=1:1时该反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是
A.原子半径由小到大的顺序为![]()
B.X的简单氢化物的热稳定性比W的强
C.化合物YX、![]() 、
、![]() 中化学键的类型相同
中化学键的类型相同
D.W的最高价氧化物对应水化物的酸性比Z的弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用NaOH固体配制250 mL 1.25 mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制250 mL 1.25 mol/L的NaOH溶液
应称取NaOH的质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它玻璃仪器 |
__________ | __________ | __________ |
(2)容量瓶上需标有以下五项中的__________;
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)__________;
A、用30 mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水(约30 mL),用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是__________,溶液注入容量瓶前需恢复到室温,这是因为__________
(5)下列配制的溶液浓度偏低的是(_____)
A.称量NaOH时,砝码错放在左盘
B.向容量瓶中转移溶液时(实验步骤②)不慎有液滴洒在容量瓶外面
C.加蒸馏水时不慎超过了刻度线
D.定容时俯视刻度线
E.配制前,容量瓶中有少量蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种药物合成中间体,其合成路线如图:
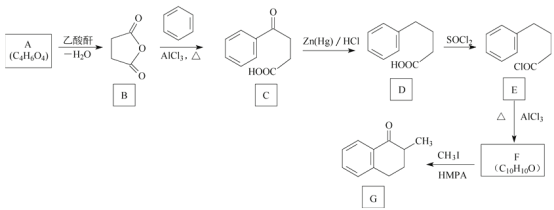
已知A分子中只含有一种官能团且能与![]() 反应生成
反应生成![]() 。回答下列问题:
。回答下列问题:
(1)A的化学名称是___________。
(2)C中的官能团名称是___________。
(3)D生成E的反应类型是___________。
(4)F的结构简式是___________。
(5)A与乙二醇在催化剂作用下反应生成可生物降解型聚酯PES,该反应的化学方程式为_________。
(6)X是G的同分异构体,满足下列条件的X共有___________种(不考虑立体异构)
①含苯环且苯环上只有三个取代基;
②含醛基且与苯环直接相连;
③除苯环外不含其他环状结构。
若①改成含苯环且苯环上只有二个取代基,其他条件不变,其中核磁共振氢谱有5组峰,面积比为6∶2∶2∶1∶1的是________(写结构简式)。
(7)由苯和甲苯制备![]() 的合成路线如下:
的合成路线如下:
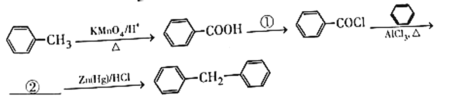
填写:①___________②___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】120℃时,将0.1 mol 氢气、2.8 g一氧化碳和0.05 mol 氮气的混合气体与足量氧气充分燃烧后,立即将所得混合气体通过足量的过氧化钠粉末,固体质量增加
A.2.8 gB.3.0 gC.7.2 gD.5.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通常利用SiO2 和碳反应来制取硅,写出反应的化学方程式___________________。
工业上还可以利用镁制取硅,反应为2Mg+SiO2 = 2MgO+Si,同时会发生副反应:2Mg + Si = Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:

(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
a.石灰石 b.锌粒 c.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 ___________________________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃.用化学方程式表示这两个反应①________________________②___________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热蒸干氯化镁溶液时因水解不完全会得到一种灰白色沉淀一一碱式氯化镁,化学式可表示为Mgx(OH)yClznH2O.设计如图装置验证其化学式。下列有关实验说法不正确的是( )

A.碱式氯化镁受热分解可以产生氧化镁,氯气和水
B.结束反应时,先停止加热,通一段时间N2后再关闭活塞K
C.①②中依次盛装氢氧化钠溶液、浓硫酸
D.只需称取原样品质量、反应结束后硬质玻璃管中剩余固体质量以及装置①增重的质量即可推出其化学式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向淀粉溶液中加适量20%H2SO4溶液,加热,冷却后加NaOH溶液至中性,再滴加少量碘水,溶液变蓝 | 淀粉未水解 |
B | 室温下,向 | 镁与盐酸反应放热 |
C | 室温下,向浓度均为 | 白色沉淀是BaCO3 |
D | 向 | H2O2具有氧化性 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com