
| A. | 太阳能、氢能、风能、生物质能都属于新能源 | |
| B. | 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H<0 | |
| C. | 人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,某物质的热值越高则其标准燃烧热越大 | |
| D. | 镀层破损后,马口铁比白铁更耐腐蚀 |
分析 A.太阳能、潮汐能、风能、氢能、生物质能等都是可再生、无污染的新能源;
B.反应不能自发,应满足△G=△H-T•△S>0;
C.1kg某种燃料完全燃烧放出的热量叫做这种燃料的热值.热值是燃料的一种特性,它只与燃料的种类有关,与燃料的质量、燃烧程度、放出热量的多少以及燃烧温度的高低等均无关;
D.根据金属的活泼性判断,Fe作负极被腐蚀,作正极被保护.
解答 解:A.太阳能、氢能、生物质能都属于新能源,故A正确;
B.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,该反应的△S>0,反应不能自发,则△G=△H-T•△S>0,所以△H>0,故B错误;
C.某物质的热值高,其标准燃烧热不一定大,故C错误;
D.Zn的活泼性比Fe强,所以构成原电池时Fe作正极被保护;Sn的活泼性比Fe弱,构成原电池时,Fe作负极被腐蚀,所以镀层破损后,白铁(镀锌铁板)比马口铁(镀锡铁板)更耐腐蚀,故D错误.
故选A.
点评 本题考查了新能源、焓变的问题以及金属的电化学腐蚀等,题目难度中等,注意自发反应满足△G=△H-T•△S>0.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
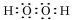 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用分液漏斗、容量瓶前都应先检漏 | |
| B. | 用托盘天平可以称取25.12g NaCl固体 | |
| C. | 仰视量筒刻度线量取浓硫酸配成的稀硫酸浓度偏高 | |
| D. | 不用任何试剂可以鉴别开NaOH、MgSO4、Ba(NO3)2、Cu(NO3)2、KNO3 五种溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2 mol HI | 1mol H2+1mol I2 | 2mol HI+1mol H2+1mol I2 |
| HI的浓度 | c1 | c2 | c3 |
| 反应的能量变化 | 吸收akJ | 放出bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | a1 | a2 | a3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1000mL水中所含K+、SO42-总数为0.15NA | |
| B. | 500mL溶液中含有0.1NA个K+ | |
| C. | 1L溶液中K+的浓度为0.1mol/L | |
| D. | 1L溶液中SO42-的浓度是0.2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HOCH2COOH既可以发生取代反应又可以发生缩聚反应 | |
| B. | 蔗糖、纤维素的水解过程都是高分子转化为小分子的过程 | |
| C. | 甲烷、甲醛、甲酸都不存在同分异构体,则甲醚(CH3OCH3)也无同分异构体 | |
| D. | 按系统命名法,化合物 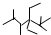 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验编号 | XOH物质的量浓度(mol•L-1) | 盐酸物质的量浓度(mol•L-1) | 混合溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | b | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com