
| A. | 铁与稀硝酸 | B. | 铁和硫酸铜溶液 | ||
| C. | 铁和氢氧化钠溶液 | D. | 铁粉与灼热的水蒸气 |
分析 A、稀硝酸具有强氧化性可以和铁发生氧化还原反应;
B、铁的活泼性大于铜,发生置换反应;
C、铁和氢氧化钠溶液不反应;
D、铁和灼热的水蒸气反应生成四氧化三铁和氢气;
解答 解:A、稀硝酸具有强氧化性可以和铁发生氧化还原反应,Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,故A不符合;
B、铁的活泼性大于铜,发生置换反应,发生的反应为:Fe+CuSO4=Cu+FeSO4,故B不符合;
C、铁和氢氧化钠溶液不反应,故C符合;
D、铁和灼热的水蒸气反应生成四氧化三铁和氢气,反应的化学方程式为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,故D不符合;
故选C.
点评 本题考查了铁的性质分析应用,主要是物质性质的熟练掌握,掌握基础是解题关键,题目较简单.


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:填空题
 为了证明铜与稀硝酸反应产生一氧化氮,某校同学设计了一个 实验,其装置如图所示(加热装置和固定装置均已略去).
为了证明铜与稀硝酸反应产生一氧化氮,某校同学设计了一个 实验,其装置如图所示(加热装置和固定装置均已略去).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3、Cl2、H3PO4 | B. | AgCl、Ba(OH)2、H2S | ||
| C. | H2SO3、NaOH、H2SO4 | D. | NH3•H2O、H2O、CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不能跟酸反应的氧化物一定能跟碱反应 | |
| B. | 同一主族元素的氢化物,相对分子质量越大,它的沸点一定越高 | |
| C. | 在CCl4、PCl3、HCl中各原子最外层均能达到8电子稳定结构 | |
| D. | 升高温度可以加快反应速率,其主要原因是反应物分子能量增加,活化分子百分数的增加,使有效碰撞次数增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
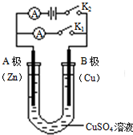 如右图所示,请按要求回答下列问题.
如右图所示,请按要求回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝属于ⅢA族元素 | B. | 铝既能溶于酸,又能溶于强碱溶液 | ||
| C. | 在常温下,铝不能与氧气反应 | D. | 铝是地壳中含量最多的金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量MgCl2、Ba(OH)2和HCl溶液混合:Mg2++3OH-+H+═Mg(OH)2↓+H2O | |
| B. | 由水电离出来的C(OH-)=10-13mol/L的溶液中加入铝粉:2Al+6H+═3H2↑+2Al3+ | |
| C. | 硝酸铁溶液中滴加足量HI溶液:Fe3++3NO3-+12H++10I-═Fe2++5I2↓+3NO↑+6H2O | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com