
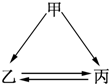
 \如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
\如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
分析 甲能发生反应生成乙和丙,说明甲反应时与甲的量或浓度或反应条件有关,乙和丙能相互转化,说明二者之间有元素化合价变化或能通过复分解反应相互转化,然后采用代入法解答.
解答 解:①假设甲是铁,铁和过量稀硝酸反应生成硝酸铁,和少量稀硝酸反应生成硝酸亚铁,硝酸亚铁和硝酸铁能相互转化,故①正确;
②假设甲是硝酸,硝酸和少量铁反应生成硝酸铁,和过量铁反应生成硝酸亚铁,硝酸铁和硝酸亚铁能相互转化,故②正确;
③假设甲是钠,钠和水反应生成氢氧化钠,钠在氯气中燃烧生成氯化钠,氢氧化钠和盐酸反应生成氯化钠,电解饱和氯化钠溶液得到氢氧化钠,故③正确;
④假设甲是硅,硅和氧气反应生成二氧化硅,不能一步实现转化关系,故④错误;
故选A.
点评 本题考查了物质的推断,明确物质的性质是解本题关键,再结合物质之间的转化来分析解答,根据物质中有变价元素为题眼来分析,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ②③ | C. | ④⑤ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2 H2O | B. | NH3 BCl3 | C. | PCl3 CH4 | D. | PCl5 CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
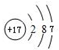 .
.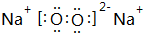 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
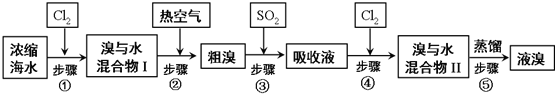
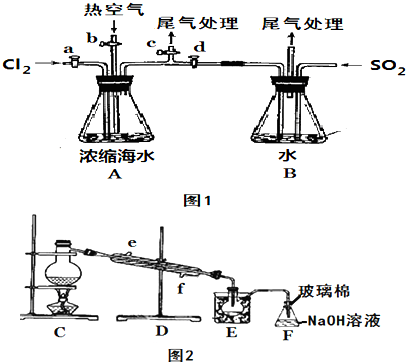
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100ml 2mol/LFeCl3溶液 | B. | 75ml 1mol/LMgCl2溶液 | ||
| C. | 150ml 3mol/LKCl溶液 | D. | 25ml 2mol/LAlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
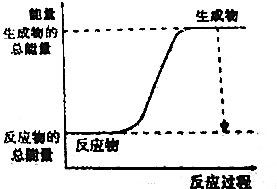
| A. | H2+Cl2$\frac{\underline{\;光照\;}}{\;}$2HCl | B. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | ||
| C. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | D. | 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
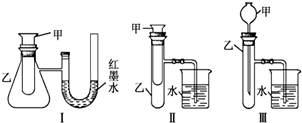
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com