
| A. | 分解温度:CH4>H2S | B. | 氧化性:NaClO>Na2SO3 | ||
| C. | 同浓度溶液pH:Na2SiO3>Na2CO3 | D. | 金属性:Ca>Na |
分析 A.元素的非金属性越强,氢化物越稳定;
B.氧化性取决于得电子能力的强弱;
C.最高价氧化物的水化物酸性越强,对应的盐碱性越弱;
D.失去电子的能力越强,元素的金属性越强.
解答 解:A.元素的非金属性越强,氢化物越稳定,稳定性硫酸氢大于甲烷,故A错误;
B.氧化性取决于得电子能力的强弱,次氯酸钠氧化性强是因为氯元素化合物为+1价,很容易得到电子,与在周期表的位置无关,故B错误;
C.最高价氧化物的水化物酸性越强,对应的盐碱性越弱,酸性:硅酸<碳酸,同浓度溶液pH:Na2SiO3>Na2CO3,故C正确;
D.失去电子的能力越强,元素的金属性越强,但金属性Ca>Na,不能从周期表的位置预测,故D错误.
故选:C.
点评 本题考查学生根据信息解决问题的能力,要求掌握扎实的基础知识,并能灵活应用,该题学生非常容易出错.


科目:高中化学 来源: 题型:选择题
| A. | 62g白磷中含有2NA个白磷分子 | |
| B. | 1L 0.2mol/L Ba(NO3)2溶液中含有0.2NA个NO3- | |
| C. | 标准状况下,用MnO2和浓盐酸反应制取Cl2,当有4mol HCl被氧化时,生成2NA Cl2 | |
| D. | 25℃时,pH=7的NH4Cl和NH3•H2O的混合溶液中,0H-数10-7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:a>b>c>d | B. | 离子半径:C(n+1)->Dn->A(n+1)+>Bn+ | ||
| C. | 单质还原性:B>A,氧化性:D>C | D. | 原子半径:A>B>C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定含有NaHCO3 | B. | 一定含有K2CO3 | C. | 可能含有NaHCO3 | D. | 一定含有NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
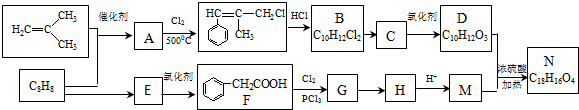
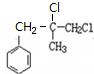 .
.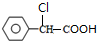 +2NaOH $→_{△}^{水}$
+2NaOH $→_{△}^{水}$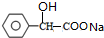 +NaCl+H2O.其反应类型为水解反应、中和反应.
+NaCl+H2O.其反应类型为水解反应、中和反应.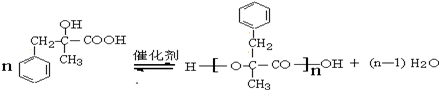 .
.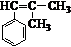 ,而不是
,而不是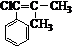 或
或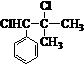 的原因是因为该条件下与双键相连的甲基上的氢原子更易取代.
的原因是因为该条件下与双键相连的甲基上的氢原子更易取代.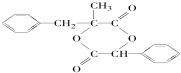 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
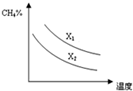 CO和H2的混合气体俗称合成气,是一种重要的工业原料气,工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.
CO和H2的混合气体俗称合成气,是一种重要的工业原料气,工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.| 浓度(mol/L) 物质 时间/min | 0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2 | 0.13 | 0.1 | 0.1 | 0.09 |
| H2 | 0 | 0.21 | 0.3 | 0.3 | 0.33 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
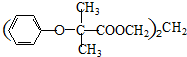
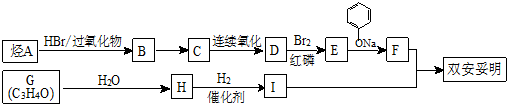
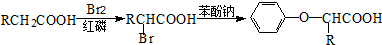
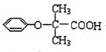 .
.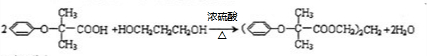 .
. .
.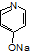 (
(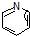 与
与 苯环性质相似)与
苯环性质相似)与 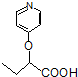 合成的路线:
合成的路线: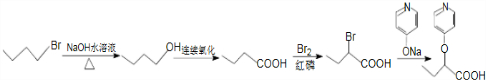 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com