
|
已知热化学方程式 CaCO3(s) | |
| [ ] | |
A. |
吸热 44.55 kJ |
B. |
吸热 89.1 kJ |
C. |
放热 44.55 kJ |
D. |
放热 89.1 kJ |
科目:高中化学 来源: 题型:
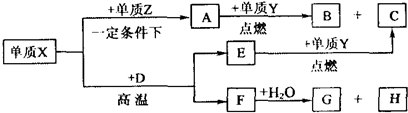




查看答案和解析>>
科目:高中化学 来源: 题型:
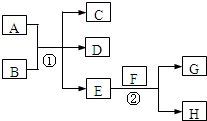 已知常温下E为无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已略),请回答下列问题:
已知常温下E为无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已略),请回答下列问题: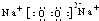
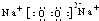
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省扬州市高三下学期5月考前适应性考试化学试卷(解析版) 题型:填空题
由菱镁矿(主要成分为MgCO3)制阻燃型氢氧化镁的工艺流程如下:
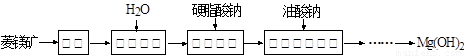
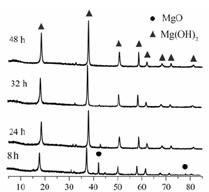
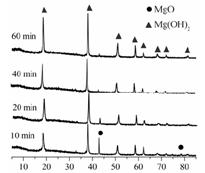


(1)从图可以得出的结论为 、 。
(2)水化反应MgO+H2O = Mg(OH)2能自发进行的原因是 。
(3)结合元素周期律和表1可知,金属氢氧化物受热分解的规律有 。(写一条即可)
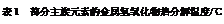
|
LiOH |
NaOH |
KOH |
Al(OH)3 |
Mg(OH)2 |
Ca(OH)2 |
Ba(OH)2 |
|
924 |
不分解 |
不分解 |
140 |
258 |
390 |
700 |
(4)已知热化学方程式:Mg(OH)2 (s) =" MgO" (s)+H2O (g) ΔH =" 81.5" kJ·mol-1
①Mg(OH)2起阻燃作用的主要原因是 。
②与常用卤系(如四溴乙烷)和有机磷系(磷酸三苯酯)阻燃剂相比,Mg(OH)2阻燃剂的优点是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com