
| A. | 所有烷烃分子中均含有碳碳单键 | |
| B. | 苯及其同系物、醇类和羧酸都能发生取代反应 | |
| C. | 大气臭氧层的破坏主要与氟氯烃的氟原子有关 | |
| D. | 氨基酸与酸、碱都能发生反应生成盐 |
分析 A.甲烷中只含有1个C;
B.苯以及同系物均能发生取代反应,醇类和羧酸能发生酯化反应;
C.氟氯烃等制冷剂的大量排放,是造成臭氧层破坏的主要原因;
D.氨基酸为两性化合物.
解答 解:A、甲烷中只含有C-H键,故A错误;
B、苯与液溴取代生成溴苯,甲苯与溴反应生成三溴甲基、羧酸与醇可以发生酯化反应,也为取代反应,故B正确;
C、氟氯烃等制冷剂的大量排放,是造成臭氧层破坏的主要原因,即与氟原子和氯原子均有关,故C错误;
D、氨基酸中含有-COOH和-NH,Wie两性化合物,既能与酸反应也能与碱反应,故D正确,故选BD.
点评 本题主要考查的是甲烷的构成、取代反应的定义、氨基酸的性质,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 油脂水解可得到丙三醇 | |
| B. | 可用碘检验淀粉是否发生水解 | |
| C. | 蛋白质水解的最终产物均为氨基酸 | |
| D. | 纤维素水解与淀粉水解得到的最终产物相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
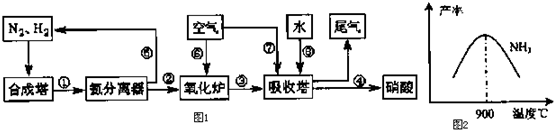
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.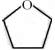 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将纤维素和硫酸加热水解后的液体取出少许,加入新制的Cu(OH)2悬浊液,并加热,若有红色沉淀生成,证明纤维素水解生成了葡萄糖 | |
| B. | 蛋白质溶液中加入甲醛可以使蛋白质从溶液中析出,加水又溶解 | |
| C. | 蔗糖和麦芽糖互为同分异物体,它们均能发生银镜反应 | |
| D. | 用甘氨酸(H2N-CH2-COOH)和丙氨酸(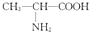 )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小 | |
| B. | 向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色 | |
| C. | 将0.001 mol•L-1的AgNO3溶液滴入KCl和KI的混合溶液中,一定先产生AgI沉淀 | |
| D. | 向AgCl的饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Ag+)=c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
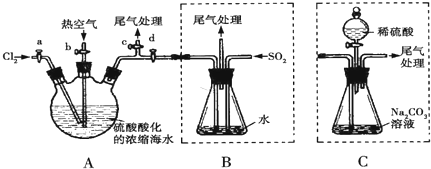
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com