


科目:高中化学 来源: 题型:
 短周期元素X、Y、Z、W在周期表中的位置如图所示,其中W的氧化物是形成酸雨的主要物质之一.
短周期元素X、Y、Z、W在周期表中的位置如图所示,其中W的氧化物是形成酸雨的主要物质之一.| X | |||
| Z | W | Y |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将纯水加热到99℃ |
| B、向水中加少量AlCl3固体 |
| C、向水中加入一小粒金属钠 |
| D、向水中加少量NaOH固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、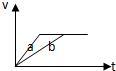 |
B、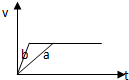 |
C、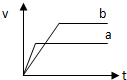 |
D、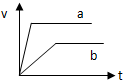 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S2- |
| B、S |
| C、SO32- |
| D、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaClO3在反应中化合价降低,得到电子,被氧化 |
| B、当反应有1mol电子转移时消耗SO2的体积为11.2L |
| C、2mol氧化剂在反应中得到2mol电子 |
| D、ClO2 是氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1s22s22p2和1s22s22p4 |
| B、1s22s22p63s23p4和1s22s22p4 |
| C、1s22s22p63s2和1s22s22p5 |
| D、1s22s22p63s1和1s22s22p63s23p4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯碱(Na2CO3) |
| B、绿 矾( FeSO4?7H2O ) |
| C、硫磺(S) |
| D、碱石灰(Ca(OH)2 ) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含金属元素的氧化物一定是碱性氧化物 |
| B、可以电离出氢离子的物质就属于酸 |
| C、物质的量是七个国际基本单位之一 |
| D、电解质的电离不需要通电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com