
分析 铁和硫酸铜反应生成硫酸亚铁和铜,根据铁片增加的质量可以计算反应的铁的质量,根据金属铁和盐酸之间的反应进行计算.
解答 解:设参加反应的铁的质量为x,析出金属铜的质量是y,
Fe+CuSO4═FeSO4+Cu,铁片增加的质量
56 64 64-56=8
x y 9.2g-8.4g=0.8g
$\frac{56}{x}=\frac{8}{0.8}$=$\frac{64}{y}$,解得x=5.6g,y=6.4g,析出金属铜物质的量是$\frac{6.4g}{64g/mol}$=0.1mol,剩余的铁片质量是8.4g-5.6g=2.8g,物质的量是0.05mol,设产生氢气物质的量是z,
Fe+2HCl=FeCl2+H2↑
1 2 1
0.05mol 0.1mol 0.05mol
所以产生气体0.05mol,消耗盐酸是0.1mol,故答案为:0.1;0.1;0.05.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求.


 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 向硫酸铵溶液中滴加氢氧化钡溶液:Ba2++SO42-=BaSO4↓ | |
| B. | 钠跟水反应:Na+2H2O=Na++2OH-+H2↑ | |
| C. | AlCl3溶液中加入过量氨水:Al3++4NH3.H2O=AlO2-+4NH4++2H2O | |
| D. | 用NaOH溶液吸收少量Cl2:Cl2+2OH-=Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 气体发生装置 |  a | 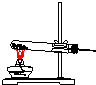 b |  c |
| 气体收集装置 |  ① |  ② |  ③ |
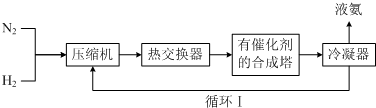
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com