
| 反应时间/min | n(CH3OH)/mol | n(CH3OCH3)/mo |
| 0 | 2.05 | 0 |
| t1 | 0.6 | |
| t2 | 0.05 |
| A. | 反应在t2 min时v正≠v逆 | |
| B. | 反应达到平衡时,放出的热量为50 kJ | |
| C. | 反应在t1 min内的平均速率为v(CH3OH)=$\frac{0.6}{{t}_{1}}$mol•L-1•min-1 | |
| D. | 若反应达到平衡后,缩小容器体积,$\frac{c(C{H}_{3}OC{H}_{3})}{c(C{H}_{3}OH)}$变大 |
分析 A.计算反应在t2 min时的浓度商,与平衡常数进行比较回答;
B.根据平衡常数进行计算生成CH3OCH3的物质的量,进而计算放出的热量;
C.根据v=$\frac{△c}{△t}$进行计算;
D.反应前后气体的体积保持不变,故改变压强对平衡无影响.
解答 解:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-25kJ•mol-1,
A.反应在t2 min时,CH3OH的物质的量浓度为$\frac{0.05mol}{2L}$=0.025mol/L,参加反应的CH3OH的物质的量浓度为$\frac{2.05-0.05}{2}$=1mol/L,故CH3OCH3的物质的量浓度为$\frac{1mol/L}{2}$=0.5mol/L,H2O的物质的量浓度为0.5mol/L,故Qc=$\frac{c(C{H}_{3}OC{H}_{3})•c({H}_{2}O)}{{c}^{2}(C{H}_{3}OH)}$=$\frac{0.5×0.5}{0.025×0.025}$=400=K,故v正=v逆,故A错误;
B.令平衡后c(CH3OCH3)=xmol/L,根据方程式可知平衡时c(CH3OH)=($\frac{2.05}{2}$-2x)=(1.025-2x)mol/L,c(H2O)=xmol/L,平衡常数K=$\frac{c(C{H}_{3}OC{H}_{3})•c({H}_{2}O)}{{c}^{2}(C{H}_{3}OH)}$=$\frac{x×x}{(1.025-2x)^{2}}$=400,解得x=0.5,则放出的热量为0.5mol/L×2L×25kJ•mol-1=25kJ,故B错误;
C.反应在t1 min内,生成CH3OH的物质的量为0.6×2=1.2mol,故v(CH3OH)=$\frac{\frac{1.2mol}{2L}}{{t}_{1min}}$=$\frac{0.6}{{t}_{1}}$mol•L-1•min-1,故C正确;
D.缩小容器体积,压强增大,平衡不发生移动,故$\frac{c(C{H}_{3}OC{H}_{3})}{c(C{H}_{3}OH)}$保持不变,故D错误;
故选C.
点评 本题考查化学平衡常数的有关计算与影响因素、化学平衡移动、化学反应中能量变化等,难度中等,根据化学平衡常数进行计算、判断反应进行方向是考查的趋势.


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 西维因是一种芳香烃 | |
| B. | 西维因分子中所有碳原子一定共面 | |
| C. | 可用FeCl3溶液检验西维因是否发生水解 | |
| D. | 在Ni催化加热条件下西维因不能与H2加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
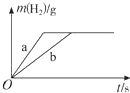
| A. | 曲线a为K,b为Na | |
| B. | 稀盐酸一定不足量 | |
| C. | 投入Na、K一定等质量 | |
| D. | 投入Na的物质的量小于K的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 周 期 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元素种类 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
| A. | 18种 | B. | 32种 | C. | 50种 | D. | 64种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 4 | ⑧ | ⑨ | ⑩ |
 ;其中心原子采取sp3杂化,空间构型为正四面体.
;其中心原子采取sp3杂化,空间构型为正四面体.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 丙烷是液化石油气的主要成分,在燃烧时能放出大量的热,作为能源广泛应用于生产和日常生活中.
丙烷是液化石油气的主要成分,在燃烧时能放出大量的热,作为能源广泛应用于生产和日常生活中.| 容器 编号 | 起始时各物质 的物质的量/mol | 达到平衡 的时间/min | 达到平衡时 体系能量的 变化/kJ | |||
| CO | H2O | CO2 | H2 | |||
| A | 1.5 | 1.9 | 0 | 0 | ta | 放出热量:36.9 |
| B | 3 | 3.8 | 0 | 0 | tb | 放出热量:Q |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com