T℃时,向1L固定体积的密闭容器M中加入2mol X和1mol Y,发生反应:2X(g)+Y(g)?aZ(g)+W(g)△H=-Q kJ/mol(Q>0);该反应达到平衡后,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小.请回答下列问题:
(1)化学计量数a的值为
(2)下列能说明该反应达到了化学平衡状态的是
(填序号).
a.容器内压强一定 b.容器内气体的密度一定
c.容器内Z的浓度一定 d.容器内气体的质量一定
(3)维持T℃温度不变,若起始时向容器M中加入4mol X和6mol Y,反应达到平衡时容器内的压强为起始压强的85%,则X的转化率为
(4)维持T℃度不变,若在一个和原容器体积相等的恒压容器N中加入2mol X和1mol Y,发生题给反应并达到平衡,则
(填“M”或“N”)容器中的反应先达到平衡状态,容器中X的质量分数M
N(填“>”、“<”或“=”).
(5)该反应的平衡常数随温度变化的情况如表所示:
| 温度/℃ | 200 | 250 | 300 | 350 |
| 平衡常数K | 9.94 | 5.2 | 1 | 0.5 |
若在某温度下,2mol X和1mol Y在容器M中反应并达到平衡,x的平衡转化率为50%,则该温度为
.



 此烃名称为
此烃名称为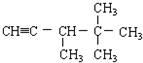 可命名为
可命名为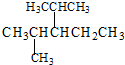 的烃可命名为:
的烃可命名为:

