
科目:高中化学 来源:不详 题型:单选题
| A.10 mL 0.5 mol·L–1 Cu(NO3)2溶液 | B.5 mL 0.8 mol·L–1 Al(NO3)3溶液 |
| C.10 mL 2 mol·L–1 AgNO3溶液 | D.10 mL 1 mol·L–1 Mg(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
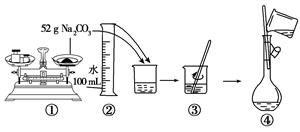
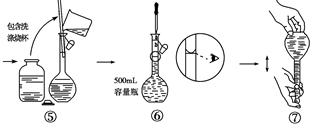
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2.3g金属钠与过量的氧气反应,无论是否加热与否转移电子数均为0.1NA |
| B.1mol Na2CO3晶体中含CO32-离子数小于NA |
| C.惰性电极电解食盐水,若线路中通过NA个电子,则阳极产生气体11.2L |
| D.0.1mol的CaO2中含阴离子数是0.2 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 B.
B. C.
C. D.
D.

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温常压下,11.2 LCH4中含有的氢原子数为2NA |
| B.标准状况下,22.4 L二氧化硫中含有氧原子数为NA |
| C.2.7 g铝与足量的盐酸反应,失去的电子数为0.3NA |
| D.1 L 0.1 mol/L MgCl2溶液中含Cl-数为0.1NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.51% | B.56% | C.49% | D.10% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com