
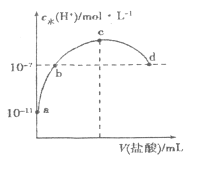
【题目】常温下,向20mL0.1![]() 氨水中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。则下列说法正确的是
氨水中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。则下列说法正确的是
A. 常温下,0.1![]() 氨水中
氨水中![]() 的电离常数K约为
的电离常数K约为![]()
B. a、b之间的点一定满足,![]()
C. c点溶液中![]()
D. d点代表两溶液恰好完全反应
【答案】A
【解析】
NH3·H2O电离出OH-抑制水的电离;向氨水中滴加HCl,反应生成NH4Cl,NH4+的水解促进水的电离,随着HCl的不断滴入,水电离的c(H+)逐渐增大;当氨水与HCl恰好完全反应时恰好生成NH4Cl,此时水电离的c(H+)达到最大(图中c点);继续加入HCl,盐酸电离的H+抑制水的电离,水电离的c(H+)又逐渐减小;据此分析。
A. 常温下,0.1mol/L的氨水溶液中水电离的c(H+)=10-11mol/L,氨水溶液中H+全部来自水电离,则溶液中c(H+)=10-11mol/L,c(OH-)=![]() mol/L=10-3mol/L,Ka=
mol/L=10-3mol/L,Ka=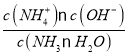 =
=![]() mol/L=1
mol/L=1![]() 10-5mol/L,所以A选项是正确的;
10-5mol/L,所以A选项是正确的;
B.a、b之间的任意一点,水电离的c(H+)<1×10-7mol/L,溶液都呈碱性,则c(H+)<c(OH-),结合电荷守恒得c(Cl-)<c(NH4+),故B错误;
C.根据图知,c点水电离的H+达到最大,溶液中溶质为NH4Cl,NH4+水解溶液呈酸性,溶液中c(H+)>10-7mol/L,c(OH-)<10-7mol/L,结合电荷守恒得: c(NH4+)<c(Cl-),故C错误;
D. 根据上述分析,d点溶液中水电离的c(H+)=10-7mol/L,此时溶液中溶质为NH4Cl和HCl,故D错误。
所以A选项是正确的。


科目:高中化学 来源: 题型:
【题目】单质硼(B)及其化合物在化学工业中有诸多用途。工业上以硼镁矿(主要成分为Mg2B2O5·H2O,还含有少量的Fe2O3、FeO)为原料制备单质B的工艺流程如图所示:
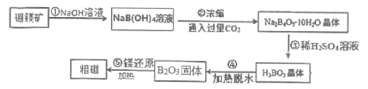
请回答下列问题:
(1)矿石中所含Fe元素在周期表中的位置_________;
(2)结合题目信息与元素周期律的有关知识,硼元素及其化合物的说法正确的是________;
A. 向碳酸氢钠溶液中滴加饱和硼酸溶液,有气泡产生
B. Al2O3为两性氧化物,可推知B2O3为两性氧化物
C. BF3分子中所有原子均达到8电子稳定结构
D. 已知硼能与NaOH溶液反应,方程式为:2B+2NaOH+6H2O=2NaB(OH)4+3H2↑
(3)上述流程中的①、②、③步骤中都用到了同一种分离方法叫___________;
(4)NaB(OH)4是硼酸的钠盐,组成该盐的四种元素原子半径由大到小的顺序为_________,硼氢化钠(NaBH4)是有机合成中的重要还原剂,其中B为+3价,NaBH4电子式_________,所含化学键类型________________;
(5)写出步骤⑤的化学方程式___________________;
(6)硼酸(H3BO3)是一元弱酸,工业上可以用电解NaB(OH)4溶液的方法来制备硼酸,同时得到氢氧化钠。其工作原理如图所示(阳离子交换膜和阴离子交换膜分别只允许阳离子、阴离子通过)。下列说法错误的是___________。
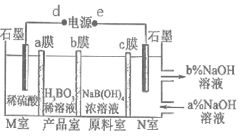
A . e与电源的负极相连接
B. 当电路中通过3mol电子时,可得到1mol H3BO3
C. 产品室中发生反应的离子方程式:H++B(OH)4-==H3BO3+H2O
D. a、c为阴离子交换膜,b为阳离子交换膜
E. M室的电极反应式为:4OH--4e-=O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中的四种元素![]() 的有关信息如下,请用合理的化学用语填写空白。
的有关信息如下,请用合理的化学用语填写空白。
在周期表中的区域 | 元素代号 | 有关信息 |
短周期元素 |
|
|
|
| |
长周期元素 |
|
|
|
|
(1)![]() 元素周期表中的位置为___________,
元素周期表中的位置为___________,![]() 、
、![]() 、
、![]() 三种元素的简单离子半径从大到小的顺序为__________。
三种元素的简单离子半径从大到小的顺序为__________。
(2)足量![]() 的最高价氧化物的水化物的稀溶液与
的最高价氧化物的水化物的稀溶液与![]() 甲完全反应,放出热量
甲完全反应,放出热量![]() ,请写出表示该过程中和热的热化学方程式____________。
,请写出表示该过程中和热的热化学方程式____________。
(3)下列有关![]() 的气态氢化物丁的说法正确的有_____________(选填字母)
的气态氢化物丁的说法正确的有_____________(选填字母)
a、丁比氯化氢沸点高 b、丁比氯化氢稳定性好
c、丁比氟化氢还原性强 d、丁比氟化氢酸性弱
(4)请写出丙溶于丁的水溶液的离子方程式____________;乙的水溶液呈酸性,请写出离子方程式解释原因_____________。
(5)![]() 是一种弱酸,请写出它的电离方程式__________________;
是一种弱酸,请写出它的电离方程式__________________;![]() 溶液有剧毒,可以用
溶液有剧毒,可以用![]() 溶液进行无毒化处理,请写出二者反应的化学方程式__________________;室温下,
溶液进行无毒化处理,请写出二者反应的化学方程式__________________;室温下,![]() 的电离常数
的电离常数![]() ,在
,在![]() 的
的![]() 溶液中滴加同浓度盐酸至溶液呈中性,此时溶液中的
溶液中滴加同浓度盐酸至溶液呈中性,此时溶液中的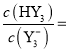 _____________。
_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(18分)从薄荷油中得到一种烃A(C10H16),叫ɑ—非兰烃,与A相关反应如下:
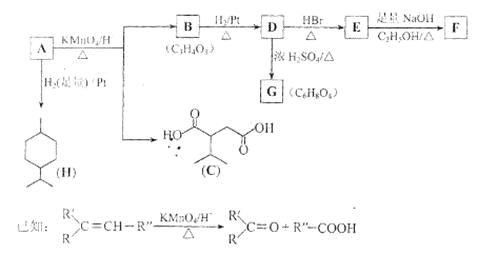
(1)H的分子式为 。
(2)B所含官能团的名称为 。
(3)含两个—COOCH3基团的C的同分异构体共有 种(不考虑手性异构),其中核磁共振氢谱呈现2个吸收峰的异构体结构简式为 。
(4)B→D,D→E的反应类型分别为 、 。
(5)G为含六元环的化合物,写出其结构简式: 。
(6)F在一定条件下发生聚合反应可得到一种高级吸水性树脂,该树脂名称为 。
(7)写出E→F的化学方程式: 。
(8)A的结构简式为 ,A与等物质的量的Br2进行加成反应的产物共有 种(不考虑立体异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下两个反应:a.NaOH+HCl=NaCl+H2O b.Cu+2Ag+ =Cu2+ +2Ag
(1)反应____(填字母)不能设计成原电池。原因是__________________________。
(2)a反应为______反应(填“放热”或“吸热”),NaOH和HCl的总能量________(填“大于”“小于”或“等于”)NaCl和H2O的总能量。
(3)已知HCl中H-Cl键的键能为431 kJ·mol-1,则断开1molH-Cl键_____431 kJ的能量,形成1molH-Cl键_____431 kJ的能量。(填“吸收”或“放出”)
(4)反应____(填字母)能设计成原电池,请画出实验装置图,注明电极材料和电解质溶液。__________

写出电极反应式及反应类型
正极反应式:_____________________,
反应类型:_______________________,
负极反应式:_____________________。
(5)上题所设计原电池中,向正极移动的离子为_______,电池工作一段时间后,电解质溶液质量减轻7.6g,正极增重的质量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于Na2CO3和NaHCO3的说法不正确的是
A.加热可除去Na2CO3固体中的NaHCO3
B.Na2CO3和NaHCO3二者在一定条件下可以相互转化
C.热稳定性:NaHCO3>Na2CO3
D.相同物质的量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体的质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g)![]() Z(g) △H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是
Z(g) △H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是
A. 以Y浓度变化表示的反应速率为0.0005 mol/(L·s)
B. 其他条件不变,将容器体积扩大至20 L,则Z的平衡浓度变为原来的1/2
C. 其他条件不变,将容器体积缩小至5L,平衡正向移动,平衡常数增大
D. 其他条件不变,升高温度逆反应速率加快,正反应速率减慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:

下列说法中正确的是( )
A.1molN2(g)和1molO2(g)完全反应放出的能量为180kJ
B.通常情况下,N2(g)和O2(g)混合能直接生成NO
C.1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)泡沫灭火器内装有NaHCO3饱和溶液,该溶液呈_________(填酸性、碱性、中性),原因(用离子方程式解释)_________________________________________;灭火器中另一容器装有Al2(SO4)3溶液,该溶液呈__________(填酸性、碱性、中性),原因(用离子方程式释)______________________________________当意外失火时,使泡沫灭火器倒过来即可使药液混合,喷出CO2和Al(OH) 3,阻止火势蔓延。原因(用离子方程式解释)__________________________________________
(2)已知25℃,AgI的饱和溶液中,c(Ag+)=1.22×10-8mol/L,AgCl的饱和溶液中,c(Ag+)=1.25×10-5mol/L。若在5ml含有KCl和KI各为0.01mol/L的溶液中,加入8ml 0.01mol/L AgNO3溶液,这时溶液中所含溶质的离子浓度由大到小的次序是_________________________________________
(3)在某温度下,将H2和I2各0.10mol的气态混合物充入10L的密闭容器中充分反应,达到平衡后,测得c(H2)=0.0080mol/L。该反应的平衡常数 K=_________;在上述温度下,该容器中若通入H2和I2蒸气各0.20mol,求达到化学平衡状态时c(H2)=___________ ,c(I2)=___________ ,c(HI)=____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com