
【题目】在Na2SO4和Al2(SO4)3的混合溶液中,测得Al3+浓度为0.1mol/L,加入等体积0.3mol/L的BaCl2溶液恰好使SO42﹣完全沉淀,则混合溶液中Na+的浓度为( )
A.0.3 mol/L
B.0.45 mol/L
C.0.6 mol/L
D.0.15 mol/L
【答案】A
【解析】解:假设溶液体积均为1L,Ba2+离子物质的量为1L×0.3mol/L=0.3mol, 混合溶液中加入BaCl2 , 恰好使溶液中的SO42﹣离子完全沉淀,则:
SO42﹣+Ba2+═BaSO4↓
0.3mol 0.3mol
c(SO42﹣)= ![]() =0.3mol/L,
=0.3mol/L,
又溶液不显电性,则有3n(Al3+)+c(Na+)=2c(SO42﹣),
故0.1mol/L×3+c(Na+)=0.3mol/L×2,
解得c(Na+)=0.3mol/L,
故选A.
Na2SO4和Al2(SO4)3的混合溶液中加入的BaCl2溶液发生反应:SO42﹣+Ba2+═BaSO4↓,假设溶液体积均为1L,根据n=cV计算Ba2+的物质的量,根据方程式计算SO42﹣的物质的量,再计算SO42﹣离子浓度,利用电荷守恒有:3n(Al3+)+c(Na+)=2c(SO42﹣),据此计算原溶液中的Na+浓度.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是 ( )
A. H2SO4 的摩尔质量是 98 g
B. Cl-的摩尔质量是 35.5 g/mol
C. 1 mol H2O 的质量是 18 g/mol
D. 1 mol氧原子的质量就是氧的相对原子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以乙炔或苯为原料可以合成有机酸H2MA,并进一步合成高分子化合物PMLA。
(一)用乙炔等有机物合成烃C。

已知:①乙炔与甲醛1:2反应生成A。
②
(1)A分子中的官能团名称是__________、__________。
(2)B转化为C的化学方程式是_________________________,其反应类型是__________。
(二)用烃C或苯合成PMLA的路线如下。

已知:![]()
(3)1mol有机物H与足量NaHCO3溶液反应生成标准状况下的CO244.8L,H有顺反异构,其反式结构简式是__________。
(4)E的核磁共振氢谱有3组峰,则E的结构简式是__________。
(5)G与NaOH溶液在加热条件下反应的化学方程式是__________。
(6)聚酯PLMA有多种结构,其中一种的主链中有-CH2-结构,写出由H2MA制该种PMLA的化学方程式______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.锌是人体健康所必需的元素,葡萄糖酸锌是一种常用的补锌剂,对婴儿及青少年的智力和身体发育有重要作用。工业上以葡萄糖酸钙为原料通过如下两步制备葡萄糖酸锌:
![]()
步骤1:充分反应后,过滤除去CaSO4沉淀。
步骤2:将葡萄糖酸溶液与ZnO混合。
(1)步骤2中,待其充分反应后,须继续加入葡萄糖酸溶液至pH为5.8,目的是_________。
(2)下列物质可替代ZnO的是______(填字母)。
a.NH3·H2O b.Zn(OH)2 c.NaOH d.ZnSO4 e.ZnCO3
Ⅱ.葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→ (C6H11O7)2 Ca (葡萄糖酸钙)+H2O+CO2
相关物质的溶解性见下表:
物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
实验流程如下:

请回答下列问题:
(3)第①步中溴水氧化葡萄糖可以用下图装置,其中水浴加热的原因是_____________。

(4)第②步中所加CaCO3还发生了其他反应,写出其中一个主要反应的方程式________;
(5)第③步需趁热过滤,原因是______________________;第④步加入乙醇的作用是______________________;
(6)第⑥步中,下列洗涤剂最合适的是________。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学科研小组研究在其他条件不变时,改变某一条件对反应[可用aA(g)+bB(g)![]() cC(g)表示]化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数):
cC(g)表示]化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数):

分析图像,回答下列问题:
(1)在图象反应Ⅰ中,若p1>p2,则此正反应为______(填“吸热”或“放热”)反应,也是一个气体分子数________(填“减小”或“增大”)的反应,由此判断,此反应自发进行必须满足的条件是________。
(2)在图象反应Ⅱ中,T1________T2(填“>”“<”或“=”),该正反应为_______(填“吸热”或“放热”)反应。
(3)在图象反应Ⅲ中,若T2>T1,则此正反应为_________________________(填“吸热”或“放热”)反应。
(4)在图象反应Ⅳ中,若T1>T2,则该反应能否自发进行?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况符合的是( )
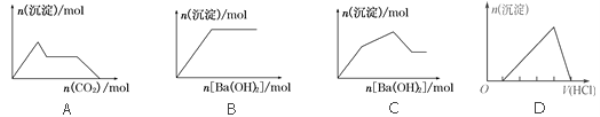
A. 向含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2至过量
B. 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量
C. 向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量
D. 向含有少量氢氧化钠的NaAlO2溶液中逐滴加入盐酸至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)广泛应用于电子、陶瓷等工业领域.在一定条件下,AlN可通过反应Al2O3+N2+3C ![]() 2AlN+3CO合成.下列叙述正确的是( )
2AlN+3CO合成.下列叙述正确的是( )
A.N2是还原剂,Al2O3是氧化剂
B.每生成1 mol AlN需转移3 mol电子
C.AlN中氮元素的化合价为+3
D.AlN的摩尔质量为41 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com