
十七大报告指出,应加强能源资源节约和生态环境保护,增强可持续发展能力。下列行为与之不相符的是
A.大量使用化学肥料,提高农作物的产量和质量
B.将作物秸秆通过化学反应转化为乙醇用作汽车燃料
C.使用资源节约型、环境友好型的生物降解塑料包装
D.推广煤炭脱硫技术、减少直接燃煤,防止酸雨发生
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
将2.32g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1 mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如下图所示,下列说法中错误的是( )
A.OA段发生反应的离子方程式为:H++OH-===H2O CO +H+===HCO
+H+===HCO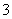
B.当加入35mL盐酸时,产生CO2的体积为224mL
C.A点溶液中的溶质为NaC1、NaHCO3
D.混合物中NaOH的质量0.60g
查看答案和解析>>
科目:高中化学 来源: 题型:
有BaCl2和NaCl混合溶液a L,将它平均分成两份,一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀。反应中消耗x mol H2SO4,y mol AgNO3。据此得知原溶液的c(Na+)为( )
A.(y-2x)/a mol·L-1
B.(y-x)/a mol·L-1
C.(2y-2x)/a mol·L-1
D.(2y-4x)/a mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
为验证碳酸氢钠固体中是否含有碳酸钠,下列实验操作及判断正确的是( )
A.观察加热时能否放出气体
B.观察滴加盐酸时能否放出气体
C.溶于水中,滴加澄清石灰水,观察是否有沉淀生成
D.溶于水中,滴加少量氯化钡溶液,观察是否有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y、Z三种元素,已知:
①X、Y、Z的单质在常温下均为气体;
②X单质在Z单质中燃烧,生成XZ,火焰为苍白色;
③每2 mol X2分子可与1 mol Y2分子化合生成2 mol X2Y分子,X2Y在常温下为液体;
④Z单质溶于X2Y中,所得溶液具有漂白作用;
⑤细铁丝能在Z2中剧烈燃烧,且产生棕色的烟。
(1)推断X、Y、Z三种元素的名称:X________,Y________,Z________。化合物的化学式为:XZ________,X2Y________。
(2)上述过程中涉及的化学反应方程式:
______________________________________________________;
______________________________________________________;
______________________________________________________;
______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3纳米)恢复了磁性,“钴酞菁”分子结构和性质与人体的血红素及植物体内的叶绿素非常相似。下列关于“钴酞菁”分子的说法中正确的是
A.均匀分散在水中所形成的分散系属悬浊液 B.分子直径比Na+小
C.均匀分散在水中形成的分散系能产生丁达尔效应D.“钴酞菁”分子不能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃、101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,辛烷的燃烧热为5 518 kJ·mol-1。下列热化学方程式书写正确的是( )
A.2H+(aq)+SO(aq)+Ba2+(aq)+2OH-(aq)===BaSO4(s)+2H2O(l) ΔH=-57.3 kJ·mol-1
B.KOH(aq)+1/2H2SO4(aq)===1/2K2SO4(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
C.C8H18(l)+25/2O2(g)===8CO2(g)+9H2O(g) ΔH=-5 518 kJ·mol-1
D.2C8H18(g)+25O2(g)===16CO2(g)+18H2O(l) ΔH=-5 518 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
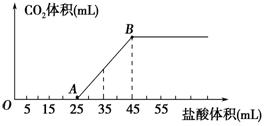
1918年,Lewis提出反应速率的碰撞理论:反应物分子间的相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起反应,只有少数碰撞才能发生化学反应。能引发化学反应的碰撞称之为有效碰撞。
(1)图①是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是________(选填“A”、“B”或“C”)。
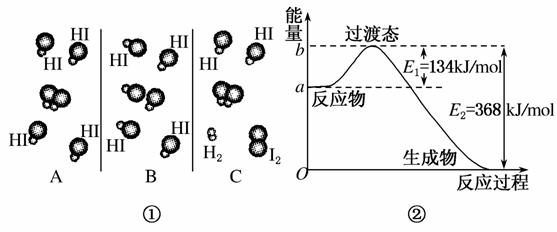
(2)20世纪30年代Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。图②是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:________________________________________________________
______________________________________________________________。
(3)过渡态理论认为,催化剂改变反应速率的原因是改变了反应的途径,对大多数反应而言主要是通过改变过渡态而导致有效碰撞所需要的能量发生变化。请在图②中作出NO2和CO反应时使用催化剂而使反应速率加快的能量变化示意图。
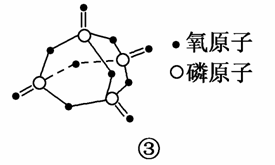
(4)进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键所需吸收的能量,下表是部分化学键的键能数据:
| 化学键 | P—P | P—O | O===O | P===O |
| 键能/kJ·mol-1 | 197 | 360 | 499 | x |
已知白磷的燃烧热为2 378.0 kJ/mol,白磷完全燃烧的产物结构如图③所示,则上表中x=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com