
| A、用盐酸和淀粉-KI试纸检验碘盐中的KIO3:IO3-+5I-+6H+=3I2+3H2O |
| B、CO(g)的燃烧热是283.0kJ?mol-1,则2CO2(g)=2CO(g)+O2(g)反应的△H=-566.0kJ?mol-1 |
| C、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| D、在某钠盐溶液中含有等物质的量的Cl-、AlO2-、CO32-、NO3-、SiO32-、I-中若干种,当加入过量的盐酸产生气泡,溶液颜色变深,阴离子种数减少3种,则原溶液中一定有CO32- |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
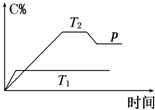 在一定条件下,可逆反应A+B?m C变化如图所示.已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:
在一定条件下,可逆反应A+B?m C变化如图所示.已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、取无水硫酸铜16 g溶于水配1L溶液 |
| B、取25 g胆矾溶于水配成1L溶液 |
| C、取16 g胆矾溶于1L水中配成 |
| D、取25 g胆矾溶于1L水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2SO3溶液(BaCl2) |
| B、FeCl2溶液(KSCN) |
| C、KI(淀粉溶液) |
| D、NaOH(BaCl2试液) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、置换、化合、分解、复分解 |
| B、化合、置换、复分解、分解 |
| C、化合、置换、分解、复分解 |
| D、置换、化合、复分解、分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com