

| A. | 图1:验证苯中是否有碳碳双键 | |
| B. | 图2:验证NaHCO3和Na2CO3的热稳定性 | |
| C. | 图3:验证溴乙烷发生消去反应生成烯烃 | |
| D. | 图4:验证酸性CH3COOH>H2CO3>C6H5OH |
分析 A.苯与溴水、高锰酸钾均不反应;
B.加热时碳酸钠不易分解、碳酸氢钠易分解;
C.乙醇也能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色;
D.强酸能和弱酸盐反应生成弱酸.
解答 解:A.苯与溴水、高锰酸钾均不反应,可验证苯中不含有碳碳双键,故A正确;
B.加热时碳酸钠不易分解、碳酸氢钠易分解,要验证NaHCO3和Na2CO3的热稳定性,如果碳酸钠的受热温度高于碳酸氢钠的受热温度,且左边烧杯中不产生白色沉淀、右边烧杯中产生白色沉淀就能验证NaHCO3和Na2CO3的热稳定性,故B正确;
C.乙醇也能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,干扰乙烯的检验,可以用溴水检验生成的乙烯,故C错误;
D.强酸能和弱酸盐反应生成弱酸,乙酸和碳酸钠反应生成二氧化碳且放出热量,导致生成的二氧化碳中含有乙酸,为防止干扰,应该除去乙酸,二氧化碳、水和硅酸钠反应生成白色沉淀硅酸,所以该实验能验证酸性CH3COOH>H2CO3>C6H5OH,故D正确;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及酸性强弱判断、物质检验、物质稳定性检验、化学键判断等知识点,明确实验原理、物质性质及其差异性是解本题关键,注意物质检验时要排除其它物质的干扰,易错选项是C.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
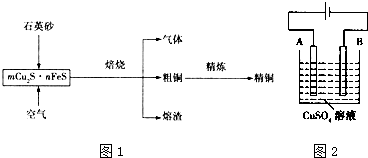
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 试验编号 | 温度(℃) | 催化剂用量(g) | 酸性高锰酸钾溶液 | 实验目的 a.实验1和2探究探究温度不同对反应速率的影响 b.实验1和3探究反应物浓度对该反应速率的影响. c.实验2和4探究催化剂对反应速率的影响 | |
| 体积(mL) | 浓度(mol•L-1) | ||||
| 1 | 25 | 0.5 | 4 | 0.1000 | |
| 2 | 50 | 0.5 | 4 | 0.1000 | |
| 3 | 25 | 0.5 | 4 | 0.0100 | |
| 4 | 25 | 0 | 4 | 0.1000 | |

| 试验编号 | 溶液褪色所需时间(min) | ||
| 第1次 | 第2次 | 第3次 | |
| 1 | 14.0 | 13.0 | 11.0 |
| 3 | 6.5 | 6.7 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
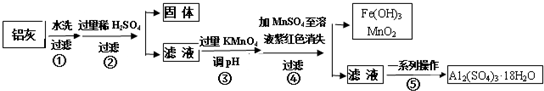
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用热的纯碱水洗手时更容易除去手上的油脂污垢 | |
| B. | 若发现厨房内天然气发生了泄漏,应立即打开门窗 | |
| C. | 用无水硫酸铜检验酒精中含有水的过程中发生了化学变化 | |
| D. | 抗战胜利70周年阅兵式上释放的气球中充入的是氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
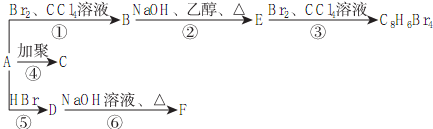
 ,D
,D ,E
,E .
.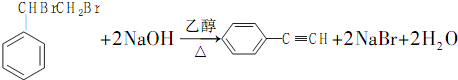 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
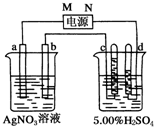 如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.
如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com