
| A. | ①③④⑦ | B. | ①②⑤⑥ | C. | ③⑤⑥⑦ | D. | ①②③④ |
分析 ①混合物由两种或两种以上的物质组成;
②纯净物由一种物质组成;
③由两种元素组成,其中一种为氧元素的化合物为氧化物;
④合金是指把金属加热熔合其他金属或非金属形成的具有金属特性的混合物;
⑤酸指电离时所有阳离子都是氢离子的化合物;
⑥碱指电离时所有阴离子都是氢氧根离子的化合物;
⑦分散质粒子直径在1nm~100nm之间的分散系属于胶体.
解答 解:①碘酒是碘的酒精溶液,酸雨是PH<5.6的雨水,都是混合物,故①正确;
②汽油和柴油都是多种烃的混合物,都是混合物,故②错误;
③冰是水的固态形式,干冰是二氧化碳的固态形式,既是纯净物又是氧化物,故③正确;
④铝合金是铝为主的合金,目前流通的硬币是用金属铸造的货币,两者都是合金,故④正确;
⑤盐酸是混合物,硫酸既是化合物又是酸,故⑤错误;
⑥纯碱属于盐,烧碱是碱,故⑥错误;
⑦豆浆和牛奶都是粒子直径在1nm~100nm之间的分散系,属于胶体,故⑦正确;
故选A.
点评 本题难度不大,考查物质类别的判别,抓住酸、碱、盐、氧化物、纯净物、混合物、合金、胶体的特征、熟悉常见的物质的组成是正确解答本题的关键.


科目:高中化学 来源: 题型:解答题
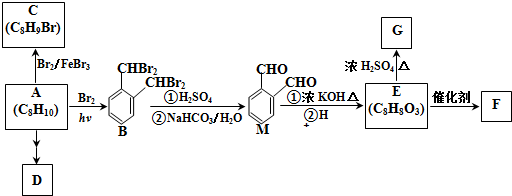

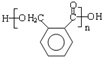 .由A生成B的反应过程中,会同时生成多种副产物,其中一种与B互为同分异构体,它的核磁共振氢谱有5个吸收峰.
.由A生成B的反应过程中,会同时生成多种副产物,其中一种与B互为同分异构体,它的核磁共振氢谱有5个吸收峰. .
.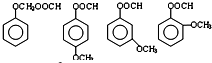 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
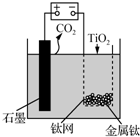 用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )
用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )| A. | 电解过程中,Ca2+向阳极移动 | |
| B. | 阳极的电极反应式为:C+2O2--4e-═CO2↑ | |
| C. | 在制备金属钛前后,整套装置中CaO的总量减少 | |
| D. | 若用铅蓄电池作该装置的供电电源,“+”接线柱是Pb电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一旦将氨气用作燃料,将彻底解决能源危机 | |
| B. | 氨气燃烧的化学方程式可能为4NH3+5O2$\frac{\underline{\;点燃\;}}{\;}$4NO+6H2O | |
| C. | 比氢气更易储存,因为氨易液化 | |
| D. | 在氨燃料电池中,氨作正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水 | B. | 加少量冰醋酸 | C. | 降低温度 | D. | 加少量烧碱溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO3溶液中加入稀硝酸:SO32-+2H+═SO2↑+H2O | |
| B. | NH4HSO3溶液与少量的NaOH溶液混合加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+2H2O | |
| C. | FeBr2溶液中通入足量的Cl2:4Fe2++4Br-+3Cl2═4Fe3++2Br2+6Cl- | |
| D. | 向碳酸氢钙溶液加入少量氢氧化钾溶液:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com