
下列说法中正确的是( )
A. 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
B. H2SO4与Ba(OH)2反应生成1mol水时放出的热叫做中和热
C. 热化学方程式中的化学计量数表示物质的量,可以是分数
D. 1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热
 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:

下列描述正确的是
A.反应开始到10 s,用Z表示的反应速率为0.158 mol·(L·s)-1
B.反应开始到10 s,X的物质的量浓度减少了0.79 mol/L
C.反应开始到10 s时,Y的转化率为79.0%
D.反应的化学方程式为:X(g)+Y(g) Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
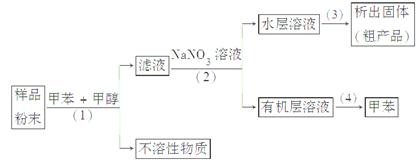
下列说法错误的是( )
A.步骤(1)需要过滤装置
B.步骤(2)需要用到分液漏斗
C.步骤(3)需要用到坩埚
D.步骤(4)需要蒸馏装置
查看答案和解析>>
科目:高中化学 来源: 题型:
某充电电池的原理如图186所 示,
示, 溶液中c(H+)=2.0 mol·L-1,阴离子为SO
溶液中c(H+)=2.0 mol·L-1,阴离子为SO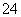 ,a、b均为惰性电极,充电时,右槽溶液的颜色由绿色变为紫色。下列对此电池叙述正确的是( )
,a、b均为惰性电极,充电时,右槽溶液的颜色由绿色变为紫色。下列对此电池叙述正确的是( )

图186
A.放电过程中,左槽溶液的颜色由黄色变为蓝色
B.充电过程中,a极的反应式为VO +2H++e-===VO2++H2O
+2H++e-===VO2++H2O
C.充电时,b极接直流电源的正极,a极接直流电源的负极
D.放电时,当转移1.0 mol电子时,共有2.0 mol H+从右槽迁移至左槽
查看答案和解析>>
科目:高中化学 来源: 题型:
M和N两溶液分别含有下列十二种离子中的五种和七种离子:K+、Na+、H+、
NH4+、Fe3+、 A13+、Cl-、OH-、NO3-、S2-、CO32-、SO42-。己知两溶液所含离子各不相同,M溶液里的阳离子只有两种,则N溶液里的阴离子应该是( )
A.OH-、CO32-、SO42- B.S2-、Cl-、SO42-
C.CO32-、NO3-、S2- D.Cl-、SO42-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
航天飞船可用肼(N2H4)和过氧化氢(H2O2)为动力源。已知1 g液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出20.05 kJ的热量。下列说法中错误的是( )
A、该反应中肼作还原剂
B、液态肼的燃烧热为20.05 kJ·mol-1
C、该动力源的突出优点之一是生成物对环境污染小
D、肼和过氧化氢反应的热化学方程式为:
N2H4(l)+2H2O2(l)===N2(g)+4H2O(g) ΔH=-641.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
有a、b、c、d四种金属。将a与b连接起来,浸入电解质溶液中,b不易腐蚀。将a、d分别投入等浓度的盐酸中,d比a反应强烈。将铜浸入b的盐溶液里,无明显变化。如果把铜浸入c的盐溶液里,有金属c析出。据此判断它们的活动性顺序由强到弱的为( )
A.a > c > d > b B.d > a > b > c
C.d > b > a > c D.b > a > d > c
查看答案和解析>>
科目:高中化学 来源: 题型:
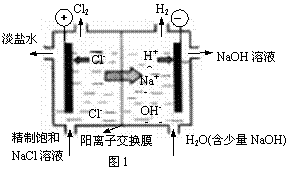
Ⅰ.氯碱工业中常用离子交换膜法电解制碱(如图1所示)。
(1)写出图1中阴极的电极反应式 。
 (2)已知阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。工业上若用图2装置电解饱和Na2SO4溶液来生产纯净的NaOH和H2SO4,则该装置最主要的缺陷是 。
(2)已知阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。工业上若用图2装置电解饱和Na2SO4溶液来生产纯净的NaOH和H2SO4,则该装置最主要的缺陷是 。

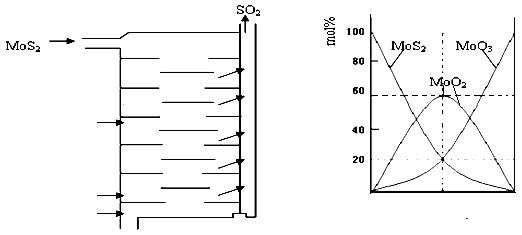
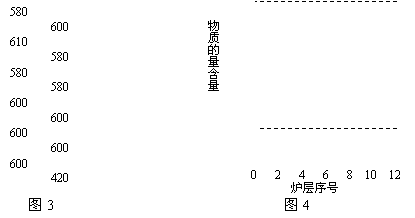
Ⅱ.辉钼矿(MoS2)是一种重要的矿物。图3是辉钼矿多层焙烧炉的示意图,其中1,2,3,…是炉层编号。580,600,610,…是各炉层的温度(℃)。图4给出了各炉层固体物料的物质的量百分含量。
|
 | |||
 | |||
(1)验证辉钼矿焙烧生成的气体是SO2而不是SO3的方法是 。
(2)辉钼矿焙烧生成的气体能使硫酸酸化的KMnO4溶液褪色,用化学方程式表示褪色的原因 。
(3)第6炉层存在的固体物质分别是MoS2、MoO3、MoO2,则它们的物质的量之比为 。
(4)图4表明,中间炉层(4~6)可能存在一种“固体+固体→固体+…”的反应,请写出该反应的热化学反应方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
 为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物和硫氧化物含量显得尤为重要。
为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物和硫氧化物含量显得尤为重要。
(1)汽车内燃机工作时会引起N2和O2的反应: ,是导致汽车尾气中含有NO的原因之一。
,是导致汽车尾气中含有NO的原因之一。
①在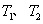 温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如右图所示,根据图像判断反应
温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如右图所示,根据图像判断反应 __________0(填“>”或“<”)。
__________0(填“>”或“<”)。
②在 温度下,向2L密闭容器中充入10molN2与5mo1O2,50秒后达到平衡,测得NO的物质的量为2mol,则该反应的速率
温度下,向2L密闭容器中充入10molN2与5mo1O2,50秒后达到平衡,测得NO的物质的量为2mol,则该反应的速率 ___________________。该温度下,若开始时向上述容器中充入N2与O2均为1 mol,则达到平衡后N2的转化率为____________。
___________________。该温度下,若开始时向上述容器中充入N2与O2均为1 mol,则达到平衡后N2的转化率为____________。
 (2)利用右图所示装置(电极均为惰性电极)可吸收SO2,用阴极排出的溶液可吸收NO2。
(2)利用右图所示装置(电极均为惰性电极)可吸收SO2,用阴极排出的溶液可吸收NO2。
①阳极的电极反应式为_____________________。
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有 生成。该反应中氧化剂与还原剂的物质的量之比为_______________。
生成。该反应中氧化剂与还原剂的物质的量之比为_______________。
(3)一定条件下可用甲醇与CO反应生成醋酸消除CO污染。常温下,将a mol·L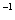 的醋酸与b mol
的醋酸与b mol L
L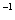
 溶液等体积混合,充分反应后,溶液中存在
溶液等体积混合,充分反应后,溶液中存在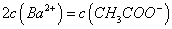 ,则该混合溶液中醋酸的电离常数Ka=______________________(用含a和b的代数式表示)。
,则该混合溶液中醋酸的电离常数Ka=______________________(用含a和b的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com