
如图,已知:①单质E可作为半导体材料;②化合物F是不能生成盐的氧化物;③化合物I能溶于水呈酸性,它能够跟氧化物A起反应.据此,请填空:
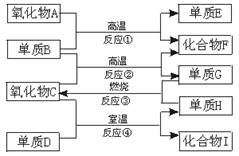
(1)化合物F是__________。(2)化合物I是__________。
(3)反应③的化学方程式是__________。(4)反应④的化学方程式__________。
(1)CO (2)HF (3)2H2+O2=2H2O (4)2F2+2H2O=4HF+O2
本题主要考查元素化合物的性质,是一道常规的框图推断题.要求学生能在全面系统地掌握元素及化合物性质的基础上,善于抓住某些元素的特殊性质为解题的突破口和切入点.
由题中所叙述的条件,单质E为半导体材料,化合物F为不成盐氧化物,结合框图中的反应①可推知E和F分别为Si和CO.反应①为:SiO2+2C=Si+2CO.氧化物A是SiO2,它除了跟氢氟酸反应以外不跟任何酸反应,由此可判断化合物I为HF.由“氧化物C+单质D→HF+单质H”可推知该反应为:2F2+2H2O=4HF+O2.至此即可突破全题。


科目:高中化学 来源: 题型:

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:鲁必修1第4章 元素与材料世界练习 题型:填空题
如图,已知:①单质E可作为半导体材料;②化合物F是不能生成盐的氧化物;③化合物I能溶于水呈酸性,它能够跟氧化物A起反应.据此,请填空: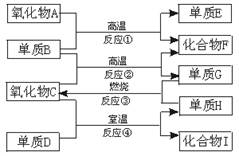
(1)化合物F是__________。(2)化合物I是__________。
(3)反应③的化学方程式是__________。(4)反应④的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
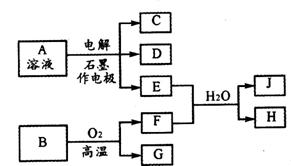
(1)电解A溶液时,两电极附近都滴入酚酞试液,通电后,使溶液变红的一极电极反应式为:__________,检验另一极电解产物最好用____________________试纸。
(2)高温煅烧12 g B,共转移电子__________mol。
(3)写出下列反应的离子方程式:E+F+H2O![]() J+H:_____________________。
J+H:_____________________。
(4)电解A溶液的总反应式为:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:

(1)化合物F是______。
(2)化合物Ⅰ是______。
(3)反应③的化学方程式是______________________________。
(4)反应④的化学方程式是______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com