
【题目】某烃类化合物A,其蒸汽对氢气的相对密度是42,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为____,名称为____。
(2)A中有多少碳原子处于同一平面____;
(3)已知A、B、C有如图转化关系:
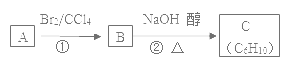
则反应②的化学方程式为___;反应的类型是____。
【答案】(CH3)2C=C(CH3)2 2,3-二甲基-2-丁烯 6 (CH3)2CBrCBr(CH3)2+2NaOH![]() CH2=C(CH3)- C (CH3) =CH2+2NaBr+2H2O 消去反应
CH2=C(CH3)- C (CH3) =CH2+2NaBr+2H2O 消去反应
【解析】
(1)A的蒸汽对氢气的相对密度是42,则A的相对分子质量为84,红外光谱表明分子中含有碳碳双键,若A为分子中只含有一个碳碳双键的单烯烃,则符合烯烃的通式CnH2n,则A的分子式为C6H12,所以A即为单烯烃,分子式为C6H12,核磁共振氢谱表明分子中只有一种类型的氢,则A为高度对称结构,所以A为(CH3)2C=C(CH3)2,根据系统命名法,A的名称为2,3-二甲基-2-丁烯;
(2)A和乙烯都是烯烃,结构相似,乙烯分子中6个原子都在同一平面上 ,A分子可以看做是乙烯分子中的4个氢原子被4个碳原子代替而生成的,所以A分子中的6个碳原子都在同一平面上;
(3)A和溴加成得到B[(CH3)2CBrCBr(CH3)2],B再在NaOH的醇溶液的作用下发生消去反应得到C:(CH3)2CBrCBr(CH3)2+2NaOH![]() CH2=C(CH3)-C(CH3)=CH2+2NaBr+2H2O。
CH2=C(CH3)-C(CH3)=CH2+2NaBr+2H2O。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】以下是工业上制取纯硅的一种方法。

请回答下列问题(各元素用相应的元素符号表示):
(1)在上述生产过程中,属于置换反应的有____(填反应代号);
(2)写出反应③的化学方程式____;
(3)化合物W的用途很广,通常可用作建筑工业和造纸工业的黏合剂,可作肥皂的填充剂,是天然水的软化剂。将石英砂和纯碱按一定比例混合加热至1 373~1 623 K反应,生成化合物W,其化学方程式是____;
(4)A、B、C三种气体在“节能减排”中作为减排目标的一种气体是___(填化学式);分别通入W溶液中能得到白色沉淀的气体是___(填化学式);
(5)工业上合成氨的原料H2的制法是先把焦炭与水蒸气反应生成水煤气,再提纯水煤气得到纯净的H2,提纯水煤气得到纯净的H2的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学设计实验制备CuBr(白色结晶性粉末,微溶于水,不溶于乙醇等有机溶剂),实验装置(夹持、加热仪器略)如图所示。
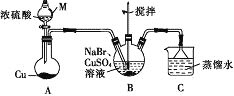
(1)仪器M的名称是________。
(2)若将M中的浓硫酸换成70%的H2SO4,则圆底烧瓶中的固体试剂为______(填化学式)。
(3)B中发生反应的化学方程式为_______,能说明B中反应已完成的依据是_____。若B中Cu2+仍未完全被还原,适宜加入的试剂是_______(填标号)。
a.液溴 b.Na2SO4 c.铁粉 d.Na2S2O3
(4)下列关于过滤的叙述不正确的是_______ (填标号)。
a.漏斗末端颈尖可以不紧靠烧杯壁
b.将滤纸润湿,使其紧贴漏斗内壁
c.滤纸边缘可以高出漏斗口
d.用玻璃棒在漏斗中轻轻搅动以加快过滤速率
(5)洗涤时,先用装置C中的吸收液清洗,其目的是_______,再依次用溶解SO2的乙醇、乙醚洗涤的目的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了制取并探究氨气的性质,按下图装置进行实验,制取氨气的原理:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O,下列说法不正确的是( )
CaCl2+2NH3↑+2H2O,下列说法不正确的是( )
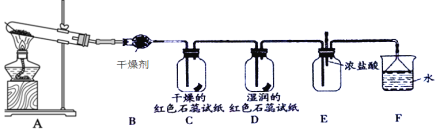
A.装置B中的干燥剂可以是P2O5B.装置C中的试纸不变色,D中试纸变蓝色
C.在装置E中滴入几滴浓盐酸会出现白烟D.装置F中的漏斗能起防倒吸作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息填空。
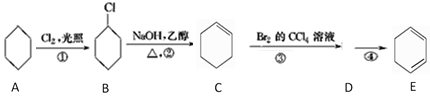
(1)A的名称是________________ ;B的分子式为______________。
(2)反应①的方程式为:________________;反应②为_______________反应;反应④的化学方程式是__________________。
(3)写出B在NaOH水溶液中加热的反应方程式:_____________,生成物官能团的名称为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将物质X逐渐加入Y溶液中,生成沉淀的物质的量n2与所加X的物质的量n1的关系如图所示,符合如图所示的情况是
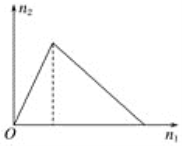
A. X为氢氧化钠,Y为氯化铝
B. X为氯化铝,Y为氢氧化钠
C. X为盐酸,Y为四羟基合铝酸钠
D. X为四羟基合铝酸钠,Y为盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe2O3和Cu2O都是红色粉末,常用作颜料.实验小组通过实验来探究某一红色粉末中Fe2O3和Cu2O的含量(不含其他物质)。
已知:Cu2O+H2SO4=Cu+Cu SO4+H2O
探究过程如下:
取少量该粉末放入 足量稀硫酸中,粉末完全溶解。
(1)①若滴加KSCN试剂后溶液不变为红色,则Fe2O3和Cu2O的物质的量之比为________。
②实验小组发现可通过对反应后溶液的称量来获得绿矾晶体(FeSO4·7H2O),设计了简单的流程来完成绿矾的制备:
混合液![]() 过滤
过滤![]() 一系列操作
一系列操作![]() 绿矾晶体(FeSO4·7H2O)
绿矾晶体(FeSO4·7H2O)
试剂a为_____________(填化学式),“一系列操作”为__________、__________、过滤、洗涤、干燥。
(2)测定Cu2O的质量分数:另取一种由Fe2O3和Cu2O组成的固体混合物9.28g,将其放在空气中充分加热(只发生Cu2O→CuO的反应),待质量不再变化时,测得质量为9.60g,则固体混合物中Cu2O的质量分数为_________________(保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在刚刚过去的一年中,发生了许多与化学相关的大事件.下列说法正确的是( )
A.被称为“史上最严”的新![]() 环境保护法
环境保护法![]() 正式实施,我们要运用化学原理从源头上减少和消除工业生产对环境的污染
正式实施,我们要运用化学原理从源头上减少和消除工业生产对环境的污染
B.天津港爆炸事故救援过程中,消防员若发现存放金属钠、电石、甲苯二异氰酸酯等化学品的仓库起火,应立即用泡沫灭火器将火扑灭
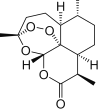
C.世界卫生组织认为青蒿素![]() 结构如图所示
结构如图所示![]() 联合疗法是当下治疗疟疾最有效的手段,烃类物质青蒿素已经拯救了上百万生命
联合疗法是当下治疗疟疾最有效的手段,烃类物质青蒿素已经拯救了上百万生命
D.某品牌化妆品在广告中反复强调产品中不含任何化学成分,是“十年专注自然护肤”的优质产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼、镁及其化合物在工农业生产中应用广泛。
Ⅰ.已知硼镁矿主要成分为Mg2B2O5H2O,硼砂的化学式为Na2B4O710H2O。一种利用硼镁矿制取金属镁及粗硼的工艺流程如图所示:
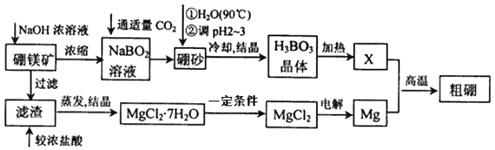
(1)写出硼元素在周期表中的位置___。
(2)将硼砂溶于热水后,用硫酸调节溶液的pH为2~3以制取硼酸H3BO3,该反应的离子方秳式为___。
(3)由MgCl27H2O制备MgCl2时,一定条件是___。
(4)制得的粗硼在一定条件下生成BI3,BI3加热分解可以得到纯净的单质硼。现将0.2000g粗硼制成的BI3完全分解,将生成的I2配制成100mL溶液,用酸式滴定管量取10mL碘水溶液放入锥形瓶中,向其中滴加几滴淀粉溶液,用0.3000molL-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液18.00mL。(提示:I2+2S2O32-=2I-+S4O6)滴定终点的现象为___,该粗硼样品的纯度为___%。
Ⅱ(5)已知:H3BO3的电离常数为5.8×10-10,H2CO3的电离常数为K1=4.4×10-7、K2=4.7×10-11。向盛有饱和硼酸溶液的试管中,滴加0.1mol/LNa2CO3溶液,__(填“能”或“不能”)观察到气泡逸出。
(6)H3BO3[也可写成B(OH)3]可以通过电解NaB(OH)4溶液的方法制备。工作原理如图所示(阳离子交换膜和阴离子交换膜分别只允许阳离子、阴离子通过)。
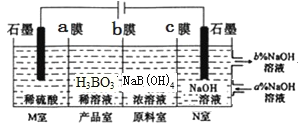
①b膜为__交换膜(填“阴离子”或“阳离子”),写出产品室发生反应的离子方程式:___理论上每生成1molH3BO3,阴极室可生成___L气体(标准状况)。
②N室中,进口和出口的溶液浓度大小关系为a%___b%(填“>”戒“<”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com