
| A. | 实验室中配制FeCl3溶液时,应向其中加入少量浓盐酸 | |
| B. | 用MgCl2•6H2O制取无水MgCl2时需在HCl气流中进行 | |
| C. | 饱和FeCl3溶液滴入沸水中可制得氢氧化铁胶体 | |
| D. | 合成氨工业中使用铁触媒做催化剂 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动,使用勒夏特列原理时,该反应必须是可逆反应且存在平衡过程,否则勒夏特列原理不适用.
解答 解:A.氯化铁是强酸弱碱盐,铁离子水解导致溶液呈酸性,配制氯化铁溶液时加入浓盐酸抑制氯化铁水解,所以可以用勒夏特里原理解释,故A不选;
B.氯化镁是强酸弱碱盐,镁离子水解导致溶液呈酸性,制取无水氯化镁时在HCl氛围中能抑制镁离子水解,所以可以用勒夏特里原理解释,故B不选;
C.氯化铁是强酸弱碱盐,铁离子水解生成氢氧化铁,且水解反应是吸热反应,升高温度促进水解,所以可以用勒夏特列原理解释,故C不选;
D.催化剂只改变反应速率不影响平衡移动,所以不能用勒夏特里原理解释,故D选;
故选D.
点评 本题考查勒夏特里原理,为高频考点,明确勒夏特里原理的适用范围是解本题关键,注意反应是否发生平衡移动,易错选项是D.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:选择题
| A. | 放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 | |
| B. | 放电时每转移3mol电子,正极有1molK2FeO4被氧化 | |
| C. | 充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O | |
| D. | 放电时正极附近溶液的碱性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸、空气、醋酸、干冰 | B. | 铁、海水、硫酸钠、乙醇 | ||
| C. | 硫酸、蔗糖、烧碱、石灰石 | D. | 胆矾、漂白粉、氯化钾、硫酸钡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
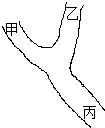 “Y”型河流上游有甲和乙两家化工厂,它们生产时都向河流排放废水.经检测,两家化工厂排出污水工有6种离子:①K+、②Ag+、③Fe3+、④Cl-、⑤OH-、⑥NO3-.某化学兴趣小组在河流下游丙处做离子检测实验,你认为该处一定可以检测到的离子是( )
“Y”型河流上游有甲和乙两家化工厂,它们生产时都向河流排放废水.经检测,两家化工厂排出污水工有6种离子:①K+、②Ag+、③Fe3+、④Cl-、⑤OH-、⑥NO3-.某化学兴趣小组在河流下游丙处做离子检测实验,你认为该处一定可以检测到的离子是( )| A. | ①和⑥ | B. | ①③⑥ | C. | ①③④⑥ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗中下层液体从下口放出,上层液体上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还需加少量蒸馏水再趁热过滤 | |
| D. | 除去混在乙酸乙酯中杂质乙酸时,可先加入饱和烧碱溶液振荡后静置,再分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的球棍模型为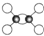 | |
| B. | H2O2的电子式为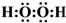 | |
| C. | 甲烷的结构式为CH4 | |
| D. | 乙酸乙酯的结构简式为CH3COOCH3CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe Cu Al Ag Mg | B. | Al Cu Mg Ag Fe | ||
| C. | Mg Cu Al Ag Fe | D. | Mg Ag Al Cu Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原溶液一定显中性 | |
| B. | 原溶液中肯定不存在的离子有Fe2+、Ba2+ | |
| C. | 无法确定原溶液中是否存在Cl-、Na+、SO42- | |
| D. | 原溶液中肯定存在的离子有Fe2+、SO42-、I- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com