
 .
.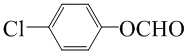 (写一种结构简式)
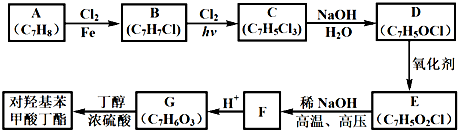
(写一种结构简式) 分析 由A的分子式为C7H8,最终合成对羟基苯甲酸丁酯可知,A为甲苯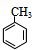 ,甲苯在铁作催化剂条件下,苯环甲基对位上的H原子与氯气发生取代反应生成B,B为
,甲苯在铁作催化剂条件下,苯环甲基对位上的H原子与氯气发生取代反应生成B,B为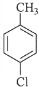 ,结合信息②可知,D中含有醛基,B在光照条件下,甲基上的H原子与氯气发生取代反应生成C,C为
,结合信息②可知,D中含有醛基,B在光照条件下,甲基上的H原子与氯气发生取代反应生成C,C为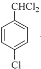 ,C在氢氧化钠水溶液中,甲基上的氯原子发生取代反应,生成D,结合信息①可知,D为
,C在氢氧化钠水溶液中,甲基上的氯原子发生取代反应,生成D,结合信息①可知,D为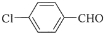 ,D在催化剂条件下醛基被氧化生成E,E为
,D在催化剂条件下醛基被氧化生成E,E为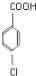 ,在碱性高温高压条件下,结合信息③可知,苯环上的Cl原子被取代生成F,同时发生酯化反应,F为
,在碱性高温高压条件下,结合信息③可知,苯环上的Cl原子被取代生成F,同时发生酯化反应,F为 ,F酸化生成对羟基苯甲酸G
,F酸化生成对羟基苯甲酸G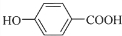 ,据此分析解答.
,据此分析解答.
解答 解:由A的分子式为C7H8,最终合成对羟基苯甲酸丁酯可知,A为甲苯 ,甲苯在铁作催化剂条件下,苯环甲基对位上的H原子与氯气发生取代反应生成B,B为
,甲苯在铁作催化剂条件下,苯环甲基对位上的H原子与氯气发生取代反应生成B,B为 ,结合信息②可知,D中含有醛基,B在光照条件下,甲基上的H原子与氯气发生取代反应生成C,C为
,结合信息②可知,D中含有醛基,B在光照条件下,甲基上的H原子与氯气发生取代反应生成C,C为 ,C在氢氧化钠水溶液中,甲基上的氯原子发生取代反应,生成D,结合信息①可知,D为
,C在氢氧化钠水溶液中,甲基上的氯原子发生取代反应,生成D,结合信息①可知,D为 ,D在催化剂条件下醛基被氧化生成E,E为
,D在催化剂条件下醛基被氧化生成E,E为 ,在碱性高温高压条件下,结合信息③可知,苯环上的Cl原子被取代生成F,同时发生酯化反应,F为
,在碱性高温高压条件下,结合信息③可知,苯环上的Cl原子被取代生成F,同时发生酯化反应,F为 ,F酸化生成对羟基苯甲酸G
,F酸化生成对羟基苯甲酸G ,
,
(1)B为 ,B的化学名称为对甲基氯苯,故答案为:对甲基氯苯.
,B的化学名称为对甲基氯苯,故答案为:对甲基氯苯.
(2)由B生成C是 在光照条件下,甲基上的H原子与氯气发生取代反应生成
在光照条件下,甲基上的H原子与氯气发生取代反应生成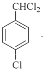 ,反应的化学反应方程式为为:
,反应的化学反应方程式为为: ;
;
(3)F为 ,分子式为C7H4O3Na2,
,分子式为C7H4O3Na2,
故答案为:C7H4O3Na2.
(4)同分异构体有两种形式,一种是苯环上含有一个酯键和一个氯原子(邻、间、对)共3种异构;另一种是有一个醛基、一个羟基和一个氯原子,这3种不同的取代基共有10种同分异构体,所以共计是13种.其中核磁共振氢谱有三种不同化学环境的氢,且峰面积比为2:2:1的是 ,
,
故答案为:13; .
.
点评 本题考查有机物合成和推断,注意根据分子式结合对羟基苯甲酸丁酯确定A的结构及发生的反应,有机合成过程主要包括官能团的引入、官能团的消除、官能团的衍变、碳骨架的变化等,需要学生熟练掌握官能团的性质,题目难度中等.


科目:高中化学 来源: 题型:选择题
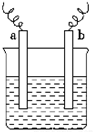 如图中,两电极上发生的电极反应如下:a极:Cu2++2e-═Cu;b极:Fe-2e-═Fe2+,则以下说法中不正确的是( )
如图中,两电极上发生的电极反应如下:a极:Cu2++2e-═Cu;b极:Fe-2e-═Fe2+,则以下说法中不正确的是( )| A. | 该装置一定是原电池 | |
| B. | a极上一定发生还原反应 | |
| C. | a、b可以是同种电极材料 | |
| D. | 该过程中能量的转换可以是电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
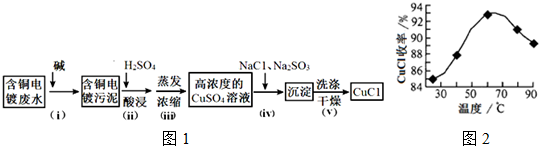
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
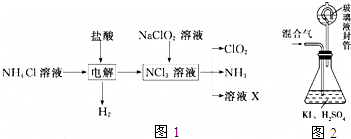
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序列 | 参加反应的物质 | 生成物 |
| ① | MnO4- … | Cl2、Mn2+ … |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 … |
| A. | 第①组反应中生成0.5mol Cl2,转移电子1mol | |
| B. | 第②组反应中Cl2与 FeBr2的物质的量之比为1:2 | |
| C. | 第③组反应的其余产物为H2O和 O2 | |
| D. | 氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| B. | 氯化铝溶液中加入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| C. | 硫酸亚铁溶液中通入足量的氯气:Fe2++Cl2═Fe3++2Cl- | |
| D. | 石灰石溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com