
在新制的氯水中加入少量的碳酸钠粉末,下列说法正确的是 ( )
A.pH增大,HClO浓度增大
B.pH减小,Cl-浓度增大
C.pH增大,Cl-浓度减小
D.pH减小,HClO浓度减小
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
如图是无机物A-M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体.D的俗名叫铁红,A是形成酸雨的主要气体。则:
(1)在周期表中,组成单质I的元素位于第 周期 族;
(2)写出S2-的离子结构示意图: ;写出N2的结构式: ;
(3)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应是 ;(填写序号)
(4)反应④的离子方程式是: 。

查看答案和解析>>
科目:高中化学 来源: 题型:
2013年12月15日4时搭载长征系列火箭的“玉兔号”顺利驶抵月球表面,实现了五星红旗耀月球的创举。火箭升空需要高能燃料,通常用肼(N2H4)作燃料,N2O4做氧化剂。请回答下列问题:
(1)已知:N2(g) + 2O2(g) == 2NO2(g) ΔH= + 67.7kJ·mol-1
N2H4(g) + O2(g)== N2(g) + 2H2O(g) ΔH= - 534.0kJ·mol-1
2NO2(g)  N2O4(g) ΔH= - 52.7kJ·mol-1
N2O4(g) ΔH= - 52.7kJ·mol-1
写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式: ;
(2)工业上用次氯酸钠与过量的氨气反应制备肼,该反应的化学方程式为: ;
(3)工业上可以用下列反应原理制备氨气:2N2(g)+6H2O(l) 4NH3(g)+3O2(g) ΔH= Q kJ·mol-1
4NH3(g)+3O2(g) ΔH= Q kJ·mol-1
 ①已知该反应的平衡常数K与温度的关系如图,则此反应的Q <
①已知该反应的平衡常数K与温度的关系如图,则此反应的Q <
0
(填“>”“<”或“=”)。
②若起始加入氮气和水,15分钟后,反应达到平衡,此时NH3的浓度为
0.3mol/L,则用氧气表示的反应速率为 。
③常温下,如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时, ABC
(选填编号).
A.容器中气体的平均相对分子质量不随时间而变化 B. v(N2)/v(O2)=2∶3
C.容器中气体的密度不随时间而变化 D.通入稀有气体能提高反应的速率
E.若向容器中继续加入N2,N2的转化率将增大
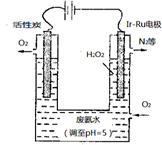 (4)最近华南理工大提出利用电解法制H2O2并以此处理废氨水,装置如图。
(4)最近华南理工大提出利用电解法制H2O2并以此处理废氨水,装置如图。
①为不影响H2O2的产量,需要向废氨水加入适量硝酸调节溶液的pH约
为5,则所得废氨水溶液中c(NH4+) c(NO3-)(填“>”“<”或
“=”);
②Ir—Ru惰性电极有吸附O2作用,该电极的电极反应为 ;
③理论上电路中每转移3mol电子,最多可以处理NH3·H2O的物质的量
为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙是三种不含相同离子的可溶性电解质。它们所含的离子如下表所示
| 阳离子 | NH |
| 阴离子 | OH-、NO |
取等质量的三种化合物配制相同体积的溶液,其物质的量浓度:c(甲)>c(乙)>c(丙),下列说法错误的是( )
A.甲中一定含Na+ B.乙中一定含NH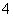
C.丙中一定含Mg2+ D.丙中一定含SO
查看答案和解析>>
科目:高中化学 来源: 题型:
某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO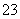 、NO
、NO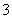 、SO
、SO 、SiO
、SiO 。
。
现进行如下实验:
Ⅰ.取少量溶液,加入KSCN溶液,无明显变化。
Ⅱ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅲ.向Ⅱ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
Ⅳ.向Ⅱ中所得的溶液中加入过量浓氨水,仅有红褐色沉淀生成。过滤,在所得滤液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成。
请回答下列问题:
(1)该废水中一定含有的离子是___________________________。
(2)实验Ⅱ中加入少量盐酸生成无色气体的离子方程式是_________________________________________________________。
(3)过滤除去Ⅳ中的蓝色沉淀,调整滤液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为14,其离子方程式为Al+NO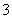 +OH-―→AlO
+OH-―→AlO +NH3+N2+H2O(未配平)。还原产物是________。若除去0.2 mol NO
+NH3+N2+H2O(未配平)。还原产物是________。若除去0.2 mol NO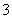 ,要消耗铝________g。
,要消耗铝________g。
(4)工业废水中常含有不同类型的污染物,可采用不同的方法处理。下列处理措施和方法中正确的是________。
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 碱性的废水 | 用CO2中和 | 化学法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含复杂有机物的废水 | 通过微生物代谢 | 物理法 |
| D | 废酸 | 加生石灰中和 | 化学法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),完成下列问题。
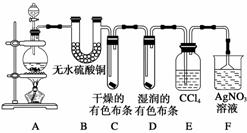
(1)装置B、E的作用分别为________,________。
(2)装置C、D的作用分别为________,________。
(3)装置F中AgNO3溶液的作用是________,倒置漏斗的作用是________。
(4)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间加一个装置。你认为该装置加在__________与________之间(填装置各部分字母),装置中应放入________,作用是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
溴化碘(IBr)的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,和某些非金属单质反应生成相应的卤化物,跟水反应的方程式IBr+H2O===HBr+HIO,下列有关IBr的叙述中,不正确的是 ( )
A.IBr是双原子分子
B.在很多反应中,IBr是强氧化剂
C.和NaOH溶液反应生成NaBr和NaIO
D.和水反应时,既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
取体积相同的KI、Na2SO3、FeBr2溶液,分别通入足量氯气,当恰好完全反应时,三种溶液消耗氯气的物质的量相同,则KI、Na2SO3、FeBr2溶液的物质的量浓度之比为( )
A.2∶1∶2 B.2∶1∶3
C.6∶3∶2 D.3∶7∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为CnH2nO2的羧酸和某醇酯化生成分子式为Cn+2H2n+4O2的酯,参加反应的羧酸和醇的质量比为1∶1,则该羧酸是
A.乙酸 B.丙酸 C.甲酸 D.乙二酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com