
【题目】硼、镁及其化合物在工农业生产中应用广泛。已知:硼镁矿主要成分为Mg2B2O5H2O,硼砂的化学式为Na2B4O710H2O,利用硼镁矿制取金属镁及粗硼的工艺流程如下,请回答下列有关问题:
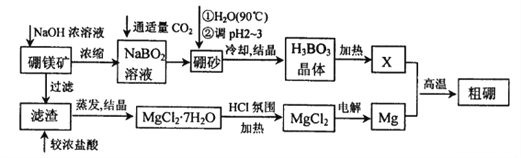
(1)硼砂中B的化合价为_________;滤渣的主要成分为_______________。
(2)X为H3BO3晶体加热脱水的产物,其与Mg制取粗硼的化学方程式为_________________________。
(3)H3BO3是一种一元弱酸,也可写作B(OH)3,它与水作用时结合水电离的OH-而呈酸性,这一变化的离子方程式为______________________________。
(4)MgCl2·6H2O需要在HCl氛围中加热,其目的是______________________。
(5)已知25℃时,Ksp[Mg(OH)2]=5.6×10-12;酸碱指示剂百里酚蓝变色的pH范围如下:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
在Mg(OH)2饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为_______________。
【答案】 +3 Mg(OH)2 3Mg+B2O3![]() 2B+3MgO H3BO3+H2O
2B+3MgO H3BO3+H2O![]() [B(OH)4]-+H+ 防止MgCl2水解生成Mg(OH)2 蓝色
[B(OH)4]-+H+ 防止MgCl2水解生成Mg(OH)2 蓝色
【解析】(1)硼砂的化学式为Na2B4O710H2O,钠元素化合价为+1价,氧元素化合价-2价,依据化合价代数和计算得到硼元素化合价为+3价;根据题意,硼镁矿(Mg2B2O5H2O)中加入氢氧化钠反应生成的滤渣用盐酸溶解后生成氯化镁,故滤渣为氢氧化镁,故答案为:+3;Mg(OH)2;
(2)X为H3BO3晶体加热脱水的产物,应为B2O3,B2O3与Mg反应制取粗硼与氧化镁,反应方程式为B2O3+3Mg![]() 2B+3MgO,故答案为:B2O3+3Mg
2B+3MgO,故答案为:B2O3+3Mg![]() 2B+3MgO;
2B+3MgO;
(3)H3BO3是一种一元弱酸,也可写作B(OH)3,它与水作用时结合水电离的OH-而呈酸性,反应的离子方程式为H3BO3+H2O![]() [B(OH)4]-+H+,故答案为:H3BO3+H2O
[B(OH)4]-+H+,故答案为:H3BO3+H2O![]() [B(OH)4]-+H+;
[B(OH)4]-+H+;
(4)MgCl27H2O需要在HCl氛围中加热,是为了防止氯化镁水解生成氢氧化镁,故答案为:防止MgCl2水解生成Mg(OH)2;
(5)25℃时,Mg(OH)2的溶度积Ksp=5.6×10-12,根据平衡Mg(OH)2(s)Mg2++2OH-可得:c(Mg2+)c2(OH-)=5.6×10-12,设c(OH-)=2c(Mg2+)=x,则:0.5x×x2=5.6×10-12,解得:x=2.24×10-4mol/L,c(H+)=![]() mol/L=4.5×10-11mol/L,溶液的pH=10.4>9.6,所以溶液呈蓝色,故答案为:蓝色。
mol/L=4.5×10-11mol/L,溶液的pH=10.4>9.6,所以溶液呈蓝色,故答案为:蓝色。


科目:高中化学 来源: 题型:
【题目】常温下,回答下列关于酸和碱中和反应的问题:
将某一元酸HA 和NaOH溶液等体积混合,分别进行编号①、②、③的实验,实验数据记录事表
序号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
① | 0.1 | 0.1 | pH=9 |
② | c | 0.2 | pH=7 |
③ | 0.2 | 0.1 | pH>9 |
请回答:
(1)根据①组实验情况,混合溶液pH=9的原因是_____________(用离子方程式表示)。
(2)混合溶液①中由水电离出的c (H+)_____0.1moI/LNaOH溶液中由水电离出的c(H+)。(填“>”“<”或“=”)
(3)根据①组实验情况,在该溶液中下列关系式正确的是(填序号字母)______。
A.c(Na+)+c(H+) =c(OH-) +c(A-)
B.c(Na+) =c(HA) +c(A-)
C.c (HA)+c(H+) =c(OH-)
D.c(Na+) +c(H+) =c(OH-) +c(A-) +c (HA)
(4)②组情况表明,c_________0.2mol/L (选填“>”、“<”或“=”)。混合溶液中离子浓度c(A-)____c(Na+) (选填“>”、“<”或“=”)。
(5)从③组实验结果分析,离子浓度由大到小的顺序是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验密为探究铁与浓硫酸(足量)的反应,并验证SO2的性质,设计如图所示装置进行实验,下列说法错误的是
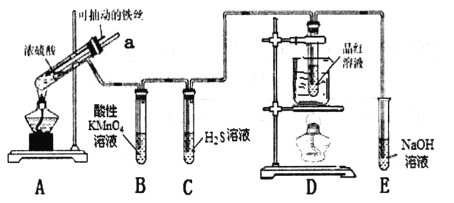
A. 装置B中酸性KMnO4溶液逐渐褪色,体现了二氧化硫的还原性
B. 实验结束后可向装置A 的溶液中滴加KSCN溶液检验是否有Fe2+
C. 装置D中品红溶液褪色可以验证SO2的漂白性
D. 实验时将导管a插入浓硫酸中,可防止装置B中的溶液倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示.又知AgCl的Ksp=1.8×10-10。下列说法不正确的是( )

A. t℃时,Y点和Z点时Ag2CrO4的Ksp相等
B. 饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点
C. t℃时,Ag2CrO4的Ksp为1×10-8
D. t℃时,将0.01mol·L-1 AgNO3溶液滴入20mL0.01mol·L-1 KCl和0.01mol·L-1 K2CrO4的混合溶液中,Cl-先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界存在丰富的碳、氮、硅、磷、铁、铜等元素,它们可形成单质及许多化合物。回答下列问题:
(1)C、N、Si原子的第一电离能由大到小的顺序是____________________。
(2)亚磷酸(H3PO3)与过量NaOH反应生成亚磷酸氢二钠(Na2HPO3),则亚磷酸的结构式为________________________。
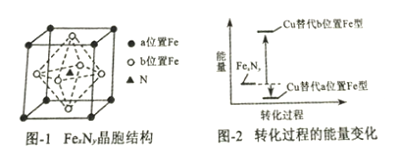
(3)某FexNy的晶胞结构如图-1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图-2所示,其中更稳定的Cu替代型产物的化学式为___________________。
(4)乙酰基二茂铁是常用汽油抗震剂,其结构如图3所示,该物质中碳原子的杂化方式有___________,亚铁离子具有强还原性,从电子排布的角度解释其原因_______________。

(5)金刚石晶胞结构如图-4,立方BN结构与金刚石相似、硬度与金刚石相当。在立方BN晶体中,B原子与N原子之间共价键与配位键数目比为____________;每个N原子周围最近且等距离的N原子数为_______________;如果阿伏加德罗常数近似取6×1023mol-1,立方BN的密度为ag·cm-3,摩尔质量为bg·mol-1,计算晶体中最近的两个N原子间距离是_________nm(用含a、b代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气中二氧化碳含量的持续增加,会产生温室效应,一种处理二氧化碳的重要方法是将二氧化碳还原,![]() ,下列说法(NA代表阿伏加德罗常数)正确的是
,下列说法(NA代表阿伏加德罗常数)正确的是
A. 2.24LCO2含有双键的数目为0.2NA
B. 1molCO2和2molH2充分反应生成CH4分子数为0.5NA
C. 通常状况下,0.1molCH4中含有的电子数为NA
D. 生成18gH2O转移电子数为8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四组离子中一定能大量共存的是 ( )
A. K+、H+、Cl﹣、CO32﹣ B. Fe3+、Mg2+、NO3﹣、SCN﹣
C. NO3﹣ H+、Fe2+、SO42﹣ D. Na+、OH﹣、Cl﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】符合如图所示的转化关系,且当X、Y、Z的物质的量相等时,存在焓变△H=△H1+△H2。满足上述条件的X、Y可能是

①C、CO ②S、SO2 ③Na、Na2O ④AlCl3、Al(OH)3 ⑤Fe、Fe(NO3)2 ⑥NaOH、Na2CO3
A. ①④⑤ B. ①②③ C. ①③④ D. ①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校课外活动小组为了探究铜与稀硝酸反应产生的是NO气体,设计了如下实验。实验装置如图所示(已知NO、NO2能与NaOH溶液反应):
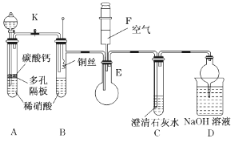
(1)设计装置A的目的是________________________________________,为达此目的应进行的操作____________________________________________________________________________;A中反应的化学方程式是_________________________________________________________。
(2)在(1)中的操作后将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是_______;B中反应的离子方程式是_________________________________________________________。
(3)装置E和F的作用是__________________________________________________________,为实现此目的,操作方法是_______________________________________________________。
(4)D装置的作用是_______________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com