
| A、CH4+2O2=CO2+2H2O△H═-889.6kJ/mol |
| B、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+889.6kJ/mol |
| C、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-55.6kJ/mol |
| D、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6kJ/mol |
| m |
| M |
| 1g |
| 16g/mol |
| 1 |
| 16 |
| m |
| M |
| 1g |
| 16g/mol |
| 1 |
| 16 |


科目:高中化学 来源: 题型:
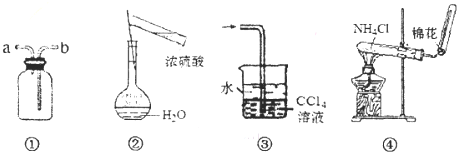
| A、装置①可用于排空气法收集NO气体 |
| B、可用图②所示装置及操作配制一定物质的量浓度的硫酸 |
| C、装置③可用于吸收氯化氢或氨气 |
| D、实验室可用装置④制取NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
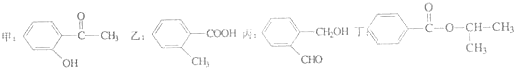
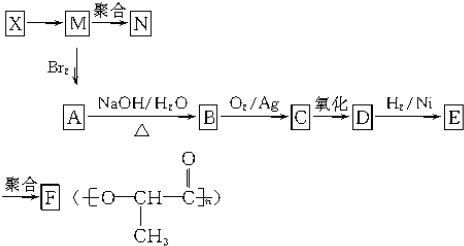
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、正极为Cu,负极为Fe,电解质溶液为FeCl3溶液 |
| B、正极为C,负极为Fe,电解质溶液为CuSO4溶液 |
| C、正极为Pt,负极为Fe,电解质溶液为CuSO4溶液 |
| D、正极为Ag,负极为Fe,电解质溶液为CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Cl-)>c(H-)>c(NH4+)>c(OH-) |
| B、c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、c(Cl-)>c(OH-)>c(NH4+)>c(H+) |
| D、c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加浓氨水 |
| B、升高温度 |
| C、加NH4Cl溶液 |
| D、加NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HS-+H+═H2S |
| B、HCO3-+H2O?H3O++CO32- |
| C、NH4++H2O?NH3?H2O+H+ |
| D、Cl2+H2O?H++Cl-+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 |
| B、50 |
| C、2.5×103 |
| D、104 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com