
下列电离或水解方程式中,正确的是
A.CH3COOH=CH3COO-+H+
B.Br-+H2O  HBr+OH-
HBr+OH-
C.CO32-+2H2O  H2CO3+2OH-
H2CO3+2OH-
D.NH4++2H2O
 NH3·H2O+H3O+
NH3·H2O+H3O+
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:




查看答案和解析>>
科目:高中化学 来源:2015届广东省肇庆市高二上学期末考试化学试卷(解析版) 题型:选择题
下列电离或离子方程式正确的是
A.亚硫酸的电离:H2SO3
 2H++ SO3
2H++ SO3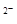
B.氯化铵水解的离子方程式为: NH4+
+H2O  NH3·H2O
+ H+
NH3·H2O
+ H+
C.NaHCO3水解的离子方程式为:HCO3-+H2O  CO3
CO3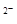 +H3O+
+H3O+
D.向氯化铝溶液中加入过量的氨水:A1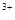 +3NH3·H2O=
Al(OH)3↓+3NH4+
+3NH3·H2O=
Al(OH)3↓+3NH4+
查看答案和解析>>
科目:高中化学 来源:新余二模 题型:问答题

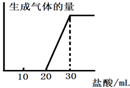
查看答案和解析>>
科目:高中化学 来源:2011年甘肃省张掖市民乐一中高考化学预测试卷(解析版) 题型:解答题
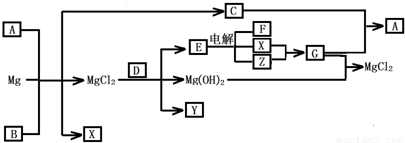
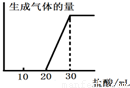
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com