

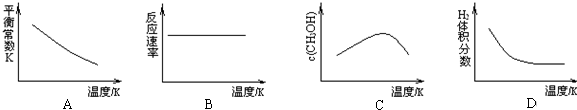
分析 (1)化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
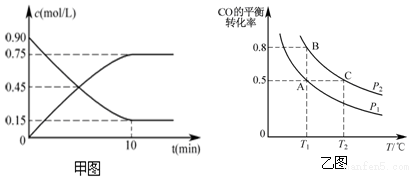
(2)图1中t2时改变条件瞬间,CO2、O2浓度不变,不能是改变浓度或改变压强,而后平衡正向移动,正反应为放热反应,降低温度平衡正向移动;
图2中t2到t3的曲线变化说明平衡没有移动,只是反应速率加快,正反应为气体体积增大的放热反应,应是使用催化剂;
(3)①反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)是熵减小的反应,△H-T△S<0能够自发进行,则正反应为放热反应,平衡后升高温度平衡逆向移动,平衡常数减小、反应速率增大、甲醇的浓度减小、氢气体积分数增大,未到平衡前,随温度升高甲醇的浓度增大、氢气体积分数减小;
②由图可知,T2先达到平衡,则温度T2>T1,又温度高时平衡状态CH3OH的物质的量少,则说明可逆反应CO2+3H2?CH3OH+H2O向逆反应方向移动,故正反应为放热反应,则T1时的平衡常数比T2时的大,故反应体系从T1变到T2,达到平衡时$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$增大,①中按照其计算速率的方法可知反应速率的单位错误,应为mol•min-1;
③根据二氧化碳的转化率计算平衡时各物质的物质的量,恒温恒容下,压强之比对气体物质的量之比.
解答 解:(1)4FeO+Cr2O3(s)+8Na2CO3(s)+7O2?8Na2CrO4(s)+2Fe2O3(s)+8CO2的化学平衡常数表达式K=$\frac{{c}^{8}(C{O}_{2})}{{c}^{7}({O}_{2})}$,故答案为:$\frac{{c}^{8}(C{O}_{2})}{{c}^{7}({O}_{2})}$;
(2)图1中t2时改变条件瞬间,CO2、O2浓度不变,不能是改变浓度或改变压强,而后平衡正向移动,正反应为放热反应,降低温度平衡正向移动;
图2中t2到t3的曲线变化说明平衡没有移动,只是反应速率加快,正反应为气体体积增大的放热反应,应是使用催化剂,
故答案为:对平衡体系降温,平衡正向移动,CO2浓度增大,O2浓度减小;b;
(3)①反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)是熵减小的反应,△H-T△S<0能够自发进行,则正反应为放热反应.
A.升温平衡逆向移动,平衡常数随温度的升高而减小,故A正确;
B.升温化学反应速率加快,故B错误;
C.达平衡后再升温,平衡逆向移动,甲醇浓度减小,故C正确;
D.达平衡后再升温,平衡逆向移动,氢气体积分数增大,故D错误;
故答案为:AC;
②A.按照其计算速率的方法可知反应速率的单位错误,应为mol•min-1,一般用单位时间内浓度变化量表示反应速率,故A错误;
B.由图可知,T2先达到平衡,则温度T2>T1,又温度高时平衡状态CH3OH的物质的量少,则说明可逆反应CO2+3H2?CH3OH+H2O向逆反应方向移动,则T1时的平衡常数比T2时的大,故B错误;
C.升高温度,平衡逆向移动,故正反应为放热反应,故C正确;
D.反应体系从T1变到T2,平衡逆向移动,则达到平衡时$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$增大,故D正确;
故答案为:CD;
③反应达到平衡后,若CO2转化率为a,则:
CO2(g)+3H2(g)=CH3OH(g)+H2O(g)
起始(mol):1 3 0 0
转化(mol):a 3a a a
平衡(mol):1-a 3-3a a a
根据相同条件下气体的压强之比等于物质的量之比,即(1-a+3-3a+a+a):(1+3)=1-$\frac{a}{2}$,
故答案为:1-$\frac{a}{2}$.
点评 本题考查化学平衡的计算,为高频考点,把握图象分析、平衡移动、化学平衡三段法为解答的关键,侧重分析与及计算能力的考查,注意图象与平衡移动原理的结合,题目难度不大.


 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:解答题
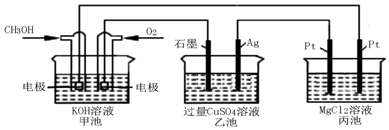
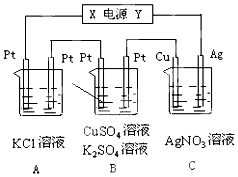 如图所示,溶液体积均为200mL,若电解5min时铜电极质量增加2.16g,试回答:
如图所示,溶液体积均为200mL,若电解5min时铜电极质量增加2.16g,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
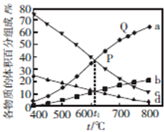 CO2与H2合成甲醚的主要反应如下:
CO2与H2合成甲醚的主要反应如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 1000 | 1115 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 名称 | 分子式 | 外观 | 沸点 |
| 高氯酸 | HClO4 | 无色液体 | 130℃ |
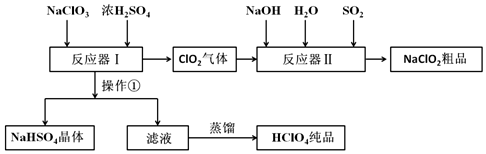
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | amol-1 | B. | 2amol-1 | C. | 4amol-1 | D. | 8a mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com