
| α |
| KW |
| A、NaOH |
| B、NaHSO4 |
| C、NH4NO3 |
| D、KCl |
| α |
| KW |
| α |
| KW |
| α |
| KW |
| α |
| KW |


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热稳定性 |
| B、常温时的溶解度 |
| C、常温时同浓度的pH |
| D、与含1mol HCl的盐酸完全反应时所需的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定条件下,1mol N2和3mol H2充分反应,生成物中的N-H键数目为6NA |
| B、1L 0.1mol?L-1的Na2S的溶液中S2-与HS-的总数为0.1NA |
| C、向含有FeI2的溶液中通入适量氯气,当有1mol Fe2+被氧化时,该反应转移电子的数目至少为3NA |
| D、1L 0.5mol?L-1 (NH4)2SO4溶液中NH4+数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
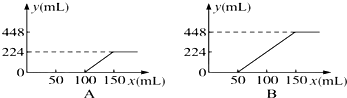
| A、在A情况下,溶质是NaOH和Na2CO3的混合物,其物质的量之比为2:1 |
| B、在B情况下,溶质是Na2CO3和NaHCO3的混合物,其物质的量之比为1:2 |
| C、在B情况下,溶质只有Na2CO3 |
| D、原NaOH溶液的物质的量浓度为1.5 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com