
���� A��B��C��D��E���ֶ�����Ԫ�ص�ԭ��������������A��Bͬ���ڣ�������AB2��DB2���ǿ�ʹ����ʯ��ˮ����ǵ����壬����������CO2��SO2�����֪AΪCԪ�أ�BΪOԪ�أ�DΪSԪ�أ�A��Cͬ���壬C��NaOH��Һ��Ӧ�ɲ�����������CΪSi��E�ĵ��ʿ���NaOH��Һ��Ӧ��E��ԭ��������������EΪCl���ݴ˽��
��� �⣺A��B��C��D��E���ֶ�����Ԫ�ص�ԭ��������������A��Bͬ���ڣ�������AB2��DB2���ǿ�ʹ����ʯ��ˮ����ǵ����壬����������CO2��SO2�����֪AΪCԪ�أ�BΪOԪ�أ�DΪSԪ�أ�A��Cͬ���壬C��NaOH��Һ��Ӧ�ɲ�����������CΪSi��E�ĵ��ʿ���NaOH��Һ��Ӧ��E��ԭ��������������EΪCl��
��1��������������֪��AΪ̼�������ڱ���λ��Ϊ���ڶ�����IVA�壬
�ʴ�Ϊ��̼���ڶ�����IVA�壻
��2��CΪSiԪ�أ�����������оƬ��̫���ܵ�أ�
�ʴ�Ϊ��������оƬ��̫���ܵ�أ�
��3��a�����¡���ѹ������������ˮ����a��ȷ��
b��OԪ���ڻ������еĻ��ϼۿ�Ϊ-1��-2�ۣ���ˮ��O����-2�ۣ�����������O����-1�ۣ���b��ȷ��
c�����ʷ���Ϊ������������������Ӻ���16�����ӡ��������Ӻ���24�����ӣ���c����
d�����������������һ�������¿��ܷ�����ը����d��ȷ��
��ѡ��abd��
��4��E����Ϊ��������NaOH��Һ��Ӧ�����ӷ���ʽ��Cl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
���� ���⿼��Ԫ�ػ������ƶϣ�ע���ʹ����ʯ��ˮ����ǵ��������ֽ����ƶϣ��ѶȲ��������ڻ���֪ʶ�Ĺ��̣�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
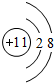 ��
��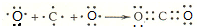 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ˮʱ����Na2SO4��Һ | |
| B�� | ��K2Cr2O7��Һ�еμ�MaOH��Һ����ɫ | |
| C�� | ʯ������ˮ��ʴ�γ��ܶ� | |
| D�� | ��TiCl4��ˮ��Ӧ�Ʊ�TiO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C14H18O5 | B�� | C14H16O4 | C�� | C16H22O5 | D�� | C16H20O5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 Al/MnO4-�����һ�ָ��ܵ�أ���Ga2O3Ϊ��ʴ������ʾ��ͼ��ͼ��ʾ����֪����ܷ�ӦΪAl+MnO4-+2H2O�TAl��OH��4-+MnO2������˵����ȷ���ǣ�������
Al/MnO4-�����һ�ָ��ܵ�أ���Ga2O3Ϊ��ʴ������ʾ��ͼ��ͼ��ʾ����֪����ܷ�ӦΪAl+MnO4-+2H2O�TAl��OH��4-+MnO2������˵����ȷ���ǣ�������| A�� | ��ع���ʱ��K+���ƶ� | |
| B�� | ��ع���ʱ��Al�缫��Χ��ҺpH���� | |
| C�� | ��ع���ʱ��������Al����Һ����Ni | |
| D�� | ������ӦΪMnO4-+2H2O+3e-�TMnO2+4OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
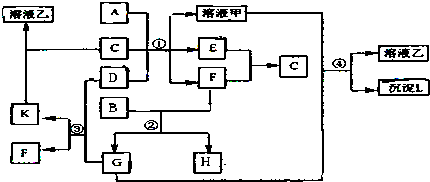
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com