
 .
. .
. .
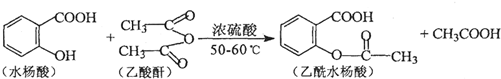
.分析 (1)根据结构简式确定乙酰水杨酸的分子式,乙酰水杨酸中只有苯环能和氢气发生加成反应;
(2)根据反应前后物质结构简式知,该反应是取代反应;
(3)A.水杨酸中不含碳碳不饱和键,不能和溴发生加成反应;
B.水杨酸含有酚羟基和羧基,能发生酯化反应;
C.酚羟基和羧基都能和氢氧化钠反应;
D.含有酚羟基,具有酚的性质;
(4)乙酰水杨酸与足量KOH溶液反应时,酯基水解生成的羧基和酚羟基都与氢氧化钠反应;
(5)乙酰氯(CH3COCl )也可以与水杨酸反应生成乙酰水杨酸,该反应是取代反应,生成乙酰水杨酸和HCl;
(6)乙酰水杨酸的同分异构体符合:Ⅰ.能遇FeCl3溶液显色,说明含有酚羟基,Ⅲ.1mol该化合物能4mol H2 反应,说明除苯环外,还含有一个双键(能与氢气发生加成反应),1mol该化合物能与4mol Br2反应,苯环上可以与3mol溴发生取代反应,Ⅱ.苯环上只有2种一溴取代物,苯环上有2种H原子,不能是2个不同的取代基处于对位,也不可能含有4个取代基,否则苯环最多与2mol溴发生取代反应,可以含有2个-OH、另外一个取代基,且均处于间位位置.
解答 解:(1)根据乙酰水杨酸的结构简式,可知其分子式为:C9H8O4,苯能与氢气发生加成反应,1mol乙酰水杨酸最多与3mol氢气发生加成反应,
故答案为:C9H8O4;3;
(2)对比反应前后物质的结构,可知水杨酸中酚羟基中H原子与乙酸酐中-OCCH3交换,属于取代反应,
故答案为:取代反应;
(3)水杨酸含有羧基,具有羧酸的性质,含有酚羟基,具有酚的性质,含有苯环,具有苯的性质;
A.水杨酸含有酚羟基,能与溴水发生取代反应,但不能与溴发生加成反应,故A错误;
B.水杨酸含有羧基,可以可发生酯化反应,不能发生水解反应,故B错误;
C.羧基、酚羟基均与氢氧化钠反应,1mol水杨酸最多能与2mol NaOH反应,故C正确;
D.含有酚羟基,遇 FeCl3溶液显紫色,故D正确,
故选:AB;
(4)乙酰水杨酸中羧基与氢氧化钾发生中和反应,酯基水解得到酚羟基与乙酸,酚羟基、乙酸与氢氧化钾发生反应,反应方程式为: ,
,
故答案为: ;
;
(5)乙酰氯(CH3COCl )也可以与水杨酸反应生成乙酰水杨酸,属于取代反应,反应同时生成HCl,反应方程式为: ,
,
故答案为: ;
;
(6)乙酰水杨酸的同分异构体符合:Ⅰ.能遇FeCl3溶液显色,说明含有酚羟基,Ⅲ.1mol该化合物能4mol H2 反应,说明除苯环外,还含有一个双键(能与氢气发生加成反应),1mol该化合物能与4mol Br2反应,苯环上可以与3mol溴发生取代反应,Ⅱ.苯环上只有2种一溴取代物,苯环上有2种H原子,不能是2个不同的取代基处于对位,也不可能含有4个取代基,否则苯环最多与2mol溴发生取代反应,可以含有2个-OH、另外一个取代基,且均处于间位位置,符合条件的一种同分异构体为: ,故答案为:
,故答案为: .
.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,注意:酯基和羧基中碳氧双键不能和氢气发生加成反应,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 氯乙烷跟化合物之间的转化如图所示:
氯乙烷跟化合物之间的转化如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该灰黑色粉末用作抗氧化剂 | B. | 小袋中的原装粉末是Fe2O3 | ||
| C. | 小袋中可能装有活性铁粉 | D. | 该灰黑色粉末不可食用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com