
�������ʵ���������ͭ�Ļ�̨��24 g��600mLϡ����ǡ����ȫ��Ӧ������NO6 .72 L(��״������Ӧ�����Һ�м���l mol��L-1 NaOH��Һʹ��������ǡ�ó��������ˡ������й�˵���������
| A��������ܽ�����Һ�� c(Fe3��)�� c(Fe2+) =1��1 |
| B�������NaOH��Һ1000mL |
| C��ϡ��������ʵ���Ũ����2 mol��L-1 |
| D��������ó����ڿ����г�ּ��ȿɵù���32 g |
B
�������������������ͭ�����ʵ�����Ϊxmol����56x+64x=24��x=0.2,��Ӧ��Cuʧȥ���ӵ����ʵ�����0.2mol��2=0.4mol�����÷�Ӧ�й�ת�Ƶ��ӵ����ʵ�����6.72L/22.4L/mol��3=0.9mol������0.2molFeʧȥ���ӵ����ʵ���Ӧ��0.9-0.4=0.5mol�����Է�Ӧ�����Һ�м��������������������ӣ��Ҷ��ߵ����ʵ���0.1mol�����Է�Ӧ�����Һ����0.1mol Fe3+��0.1molFe2+��0.2molCu2+��A��������ܽ�����Һ�� c(Fe3��)�� c(Fe2+) =1��1 ����ȷ��B����Һ�����������Ӵ��ڣ�˵���������꣬�����������������Ƶ����ʵ�����0.1mol��3+0.1mol��2+0.2mol��2=0.9mol����Ҫl mol��L-1�������Ƶ������900mL������C������NԪ���غ㣬ԭ��Һ����������ʵ�����0.1mol��3+0.1mol��2+0.2mol��2+6.72L/22.4L/mol=1.2mol������ϡ��������ʵ���Ũ����1.2mol/0.6L="2" mol��L-1����ȷ��D�������ڼ��ȹ������������ӱ�����Ϊ�����ӣ�����������ó����ڿ����г�ּ��ȵõ�������������ͭ�Ĺ��壬����ͭ�����ʵ�����0.2mol�������������ʵ�����0.1mol�����Թ��������������32g����ȷ����ѡB��
���㣺��������ͭ�Ļ�ѧ���ʣ�������ԭ��Ӧ�ļ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��һƿ��ɫ�������ϡ��Һ�������������֣����п��ܺ���SO42-��Na+��CO32-��H+��NO3-��HCO3-��Cl-�������е������֡���һ���ķ���������£�
��1����pH��ֽ�ⶨ��Һ��pH����ֽ�ʺ�ɫ������ɫ��
��2��ȡ2mL��Һ�μ�����BaCl2��Һ���а�ɫ�������ɣ��ٵμ�����ϡHNO3����������ʧ
��3���ԣ�2�������õĻ�����־��ú�ȡ�ϲ���Һ�μ�����AgNO3��Һ�����а�ɫ�������ɣ��ٵμ�����ϡHNO3����������ʧ
��1����Һ��һ�����ڵ������� ��һ�������ڵ������� ��
��2���ܷ��ж�ԭ��Һ���Ƿ���Cl- �����ǡ� �� ������ԭ��Ϊ ����Ҫȷ����Һ���Ƿ���Cl-������ȷ�IJ����� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��ij��Һ�н����±������е�5�����ӣ�������ˮ�ĵ��뼰���ӵ�ˮ�⣩�������ӵ����ʵ�����Ϊ1mol��
| ������ | SO42-��NO3-��Cl- |
| ������ | Fe3+��Fe2+��NH4+��Cu2+��Al3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
MnO2��һЩ���ʻ���;��ͼ������˵����ȷ���� ( )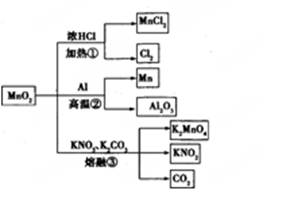
| A���١��ڡ���������Ӧ��MnO2���������� |
| B������MnO2��2 L 10 mol/LHCl���ȣ�������5 mol C12 |
| C����Ӧ��������1 mol Al2O3����Ӧ������ת��12 mol���� |
| D����Ӧ����K2CO3��KNO3�Ļ�ѧ��������Ϊ1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ݱ�����Ϣ�жϣ�����ѡ����ȷ���� �� ��
| ��� | ��Ӧ�� | ���� |
| �� | KMnO4��H2O2��H2SO4 | K2SO4��MnSO4���� |
| �� | Cl2��FeBr2 | FeCl3��FeBr3 |
| �� | MnO4������ | Cl2��Mn2+���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����£���ˮ��Һ�з������·�Ӧ���� ��
��16H++10C��+2XO4 �� = 2X2+��5C2��8H2O����2A2+��B2 = 2A3+��2B������2B����C2 = B2��2C����
����˵���������
| A����ӦC2 �� 2A2+ = 2A3+ �� 2C�� ���Խ��� |
| B����ԭ����ǿ������˳����C��>A2+>B��>X2+ |
| C����������ǿ������˳����XO4��>C2>B2>A3+ |
| D����Ӧ�����û���Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ij�Ͻ�(����ͭ����)��ͭ���������ʵ���֮��Ϊymol������Cu�����ʵ�������Ϊa ������ȫ��Ͷ��50mLbmol��L��1��������Һ�У�����ʹ���ַ�Ӧ(����NO��Ψһ�Ļ�ԭ����)������˵������ȷ����
| A����������ʣ�࣬����Һ���ٵ�����������ֿ�ʼ�ܽ� |
| B��������ȫ���ܽ⣬����Һ�в�һ������Fe3�� |
| C��������ȫ���ܽ⣬�Ҳ���336mL����(��״��)����b=0.3 |
| D������Һ�н�������ֻ��Fe3����Cu2��ʱ����a��b�Ĺ�ϵΪ��b��80y(1��a/3) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ����������ͨ��30 mLŨ��Ϊ10.00 mol/L����������Ũ��Һ�У���������ʱ�����Һ���γ�NaCl��NaClO��NaClO3������ϵ�������ж���ȷ���� (����)
| A����NaOH��Ӧ������һ��Ϊ0.3 mol |
| B��n(Na��)��n(Cl��)����Ϊ7��3 |
| C������Ӧ��ת�Ƶĵ���Ϊn mol����0.15��n��0.25 |
| D��n(NaCl)��n(NaClO)��n(NaClO3)����Ϊ11��2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������������������ԭ��Ӧ��
��2FeCl3��2KI===2FeCl2��2KCl��I2
��2FeCl2��Cl2===2FeCl3
��2KMnO4��16HCl===2KCl��2MnCl2��5Cl2����8H2O
��ij��Һ����Fe2����I����Cl�����棬Ҫ��ȥI����������Fe2����Cl������ɼ�����Լ���
| A��Cl2 | B��KMnO4 | C��HCl | D��FeCl3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com