
【题目】下列物质能用分液的方法进行分离的是
A. 汽油和煤油B. 乙醇和水
C. 乙酸和乙醇D. 乙酸乙酯和碳酸钠溶液
科目:高中化学 来源: 题型:
【题目】一定温度下,在一固定体积的密闭容器中发生反应A(s)+3B(g)2C(g),下列说法中能说明该反应达到化学平衡状态的是( )
①C的生成速率和C的分解速率相等
②单位时间内生成a mol A,同时生成3a mol B
③气体密度不再变化
④混合气体的总压强不再变化
⑤A、B、C的物质的量之比为1∶3∶2
⑥混合气体的平均相对分子质量不变
A. ②④⑤ B. ①③④⑥ C. ①②④⑥ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示仪器可用于实验室制备少量无水FeCl3 , 仪器连接顺序正确的是( ) 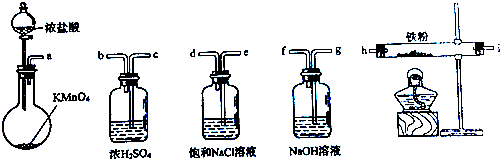
A.a﹣b﹣c﹣d﹣e﹣e﹣f﹣g﹣h
B.a﹣e﹣d﹣c﹣b﹣h﹣i﹣g
C.a﹣d﹣e﹣c﹣b﹣h﹣i﹣g
D.a﹣c﹣b﹣d﹣e﹣h﹣i﹣f
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中.请回答下列问题: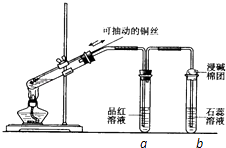
(1)写出铜与浓硫酸反应的化学方程式 .
(2)试管a、b分别检验生成气体的性质,写出观察到的现象及其作用.
试管a中的现象是 , 作用是 .
试管b中的现象是 , 作用是 .
(3)如图将铜丝改为可抽动的铜丝符合化学实验“绿色化”的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,分别向浓度均为0.1 mol·L1,体积均为20 mL的HX和HY的溶液中滴入等物质的量浓度的氨水,溶液中水电离出的c(H+)与滴入氨水的体积关系变化如图所示。下列说法正确的是
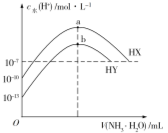
A.HX的电离方程式:HX![]() H++X
H++X
B.b点时溶液中c(![]() )=c(Y)>c(H+)=c(OH)
)=c(Y)>c(H+)=c(OH)
C.一种酸的电离平衡常数约为1×107 mol·L1
D.a、b两点对应溶液中存在的微粒种类数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表中物质分类完全正确的是 ( )
选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
A | 盐酸 | 水玻璃 | 硫酸 | 干冰 |
B | 小苏打 | 漂粉精 | 铁 | 氨气 |
C | 液氨 | 碱石灰 | 氢氧化钠 | 二氧化碳 |
D | 硝酸 | 食盐水 | 氯化铜 | 氯气 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜锌原电池装置(见图),下列分析正确的是( ) 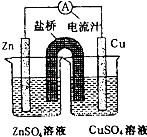
A.一段时间后两烧杯中c(Zn2+)、c(Cu2+)均减小
B.原电池工作时,Cu电极流出电子,发生氧化反应
C.原电池工作时的总反应为Zn+Cu2+═Zn2++Cu
D.盐桥中装有含氯化钾的琼脂,其作用是传递电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组采用下列装置,对浓硫酸与木炭的反应进行探究。

请回答下列问题:
(1)检查装置气密性后,将燃料匙中的木炭在酒精灯上加热至红热状态,立即伸入三颈瓶中,并塞紧瓶塞,滴加浓硝酸,可观察到三颈瓶中气体的颜色为________,产生该气体的化学反应方程式是___________。
(2)装置C中盛有足量Ba(OH)2溶液,反应一段时间后可观察到C中出现白色沉淀,该白色沉淀为_______(写化学式)。
(3)装置B的作用是________________________。
(4)装置D中收集到了无色气体,部分同学认为是NO,还有部分同学认为是O2。(假设装置内空气已排净,D瓶中收集的气体仅为产物)。
①下列对该气体的检验方法合适的是________(填序号)。
A. 敞口观察集气瓶内气体的颜色变化
B. 将润湿的蓝色石蕊试纸伸入集气瓶内,观察试纸是否变红
C. 将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果集气瓶中收集到的无色气体是氧气,则氧气的来源是___。(用相关化学方程式表示)。
(5)若将木炭改为铜片,再用等质量的铜片分别与等体积的浓硝酸、稀硝酸(硝酸均过量)反应时,发现反应后所得溶液前者呈绿色,后者呈蓝色。针对此现象,同学们进行讨论,提出两种意见:①认为两溶液所显颜色不同是由Cu2+浓度的差异引起的。②认为前者溶液呈绿色,是因为生成的红棕色NO2溶解于溶液中引起的。
你认为上述意见________ (填“①”或“②”)合理。请设计一个简单的实验进行验证:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,选用硫酸、盐酸、CaCO3、Na2SO4溶液、Na2SiO3溶液中某些试剂,设计了如图1装置来一次性完成同主族元素碳与硅的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律,A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红色试纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气. 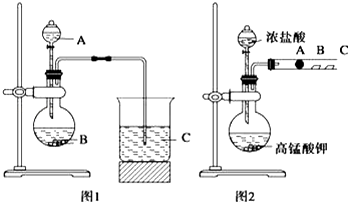
根据图1回答:
(1)写出选用物质为:A , C
(2)烧瓶中反应的离子方程式为
(3)有同学认为甲同学的实验设计有明显的不足,你认为不足之处为 .
根据图2回答:
(4)根据乙同学的实验原理可推测氯、溴、碘元素的非金属性强弱顺序为:
(5)B处的实验现象是;
(6)B处的反应的离子方程式: .
(7)有同学认为乙同学的实验设计也有明显的不足,你认为不足之处为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com