
已知下述三个实验均能发生化学反应。
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴浓硝酸 | 将铁钉放入氯化铁溶液中 |
下列判断正确的是( )
A. 实验①和③中的铁钉只作还原剂
B. 上述实验证明氧化性:Fe3+>Fe2+>Cu2+
C. 实验②中Fe2+既显氧化性又显还原性
D. 实验③中反应的离子方程式为Fe+Fe3+=2Fe2+
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:
发展混合动力车是实施节能减排的重要措施之一。混合动力车的电动机目前一般使用的是镍氢电池。汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态以节省能耗。镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液.镍氢电池充放电原理如图,其总反应式为: H2+2NiOOH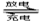 2Ni(OH)2
2Ni(OH)2
下列有关混合动力车的判断正确的是( )
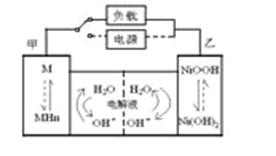
A.在上坡或加速时,每消耗22.4LH2,从电极甲流向电极乙的电子是2mol
B.在上坡或加速时,乙电极周围溶液的pH将减小
C.在刹车和下坡时,溶液中的K+向乙电极迁移
D.在刹车和下坡时,甲电极的电极反应式为2H2O+2e-=H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色.如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色.完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):
________ +________
+________ +________
+________ →________
→________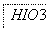 +________
+________
(2)整个过程中的还原剂是________.
(3)把KI换成KBr,则CCl4层变为________色;继续滴加氯水,CCl4层的颜色没有变 化.Cl2、HIO3、HBrO3氧化性由强到弱的顺序是________________________________.
化.Cl2、HIO3、HBrO3氧化性由强到弱的顺序是________________________________.
(4)加碘盐中含碘量为20 mg~50 mg/kg.制取加碘盐(含KIO3的食盐)1 000 kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2________L(标准状况,保留2位小数).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,反应后固体物质增重的是
A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热 反应 D.将锌粒投入Cu(NO3)2溶液
反应 D.将锌粒投入Cu(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示 仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是
仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是

A.a-b-c-d-e-e-f-g-h B.a-e-d-c-b-h-i-g
C.a-d-e-c-b-h-i-g D.a-c-b-d-e-h-i-f
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、Na+、NH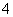 、Mg2+、Fe3+、Al3+、SO
、Mg2+、Fe3+、Al3+、SO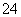 、CO
、CO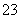 等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示,下列说法正确的是( )
等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示,下列说法正确的是( )

A.原溶液中含有的阳离子是H+、NH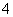 、Mg2+、Al3+
、Mg2+、Al3+
B.原溶液中一定含有SO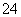 和Na+
和Na+
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1∶1
D.反应最后形成的溶液中含有的溶质只有Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
X为某金属矿的主要成分,X具有下列转化关系(部分反应物、生成物没有列出)。

已知:1 mol X经一系列变化只生成A、B、C,且物质的量之比为1∶2∶1,X不含氧元素。请回答:
(1)X的化学式为________;
(2)写出物质A名称________;物质G名称:________;
(3)写出下列反应方程式:
C+E—→B+F__________________________________;
生成红色沉淀G___________________________________
___________________________ ______________________;
______________________;
(4)工业生产纯净C的方法是________;其阴极电极反应式是:________;
(5)已知反应②的热化学方程式为:2B(g)+O2(g)2D(g) Δ<0
该反应平衡常数表达式为:________;
升高温度 K值的变化是:________。(填“变大”、“变小”或“不变”)
K值的变化是:________。(填“变大”、“变小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)0.5 mol CH4的质量是________g,在标准状况下的体积为________L;含________个氢原子。
(2)将标准状况下22.4 L的HCl溶于水配成200 mL的溶液,所得溶液的物质的量浓度为________;配制300 mL 0.5 mol·L-1氯化钠溶液,需要1.5 mol·L-1的氯化钠溶液的体积是________mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com