
”¾ĢāÄæ”æČēŗĪ½µµĶ“óĘųÖŠCO2µÄŗ¬Įæ¼°ÓŠŠ§µŲæŖ·¢ĄūÓĆCO2ŹĒµ±Ē°æĘѧ¼ŅŃŠ¾æµÄÖŲŅŖæĪĢā”£
(1)æĘѧ¼ŅÓĆH2ŗĶCO2Éś²ś¼×“¼Č¼ĮĻ”£ĪŖĢ½¾æøĆ·“Ó¦ŌĄķ£¬½ųŠŠČēĻĀŹµŃé£ŗijĪĀ¶ČĻĀ£¬ŌŚČŻ»żĪŖ2 LµÄĆܱÕČŻĘ÷ÖŠ³äČė1 mol CO2ŗĶ3.25 mol H2£¬ŌŚĪĀ¶ČŅ»¶ØµÄĢõ¼žĻĀ·“Ó¦£¬²āµĆCO2”¢CH3OH(g)ŗĶH2O(g)µÄĪļÖŹµÄĮæ(n)Ėꏱ¼äµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£
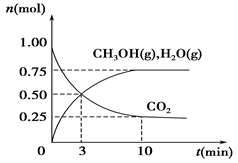
¢Ł“Ó·“Ó¦æŖŹ¼µ½3 minŹ±£¬ĒāĘųµÄĘ½¾ł·“Ó¦ĖŁĀŹv(H2)£½________”£
¢ŚĻĀĮŠ“ėŹ©ÖŠŅ»¶ØÄÜŹ¹CO2µÄ×Ŗ»ÆĀŹŌö“óµÄŹĒ________”£
A£®ŌŚŌČŻĘ÷ÖŠŌŁ³äČė1 mol CO2 B£®ŌŚŌČŻĘ÷ÖŠŌŁ³äČė1 mol H2
C£®ŌŚŌČŻĘ÷ÖŠ³äČė1 mol He D£®Ź¹ÓĆøüÓŠŠ§µÄ“߻ƼĮ
E£®ĖõŠ”ČŻĘ÷µÄČŻ»ż F£®½«Ė®ÕōĘų“ÓĢåĻµÖŠ·ÖĄė³ö
¢ŪÄÜĖµĆ÷·“Ó¦ŅŃ“ļĘ½ŗāדĢ¬µÄŹĒ________(Ģī×ÖÄø,ĻĀĶ¬)”£
A.v(H2)=3v(CO2) B.ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä
C.vÄę(CO2)=vÕż(CH3OH) D.ČŻĘ÷ÄŚĆܶȱ£³Ö²»±ä
(2)æĘѧ¼Ņ»¹ĄūÓĆĒāĘųŌŚŅ»¶ØĢõ¼žĻĀÓė¶žŃõ»ÆĢ¼·“Ӧɜ³ÉŅŅ“¼Č¼ĮĻ£¬ĘäČČ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ2CO2(g)£«6H2(g) ![]() CH3CH2OH(g)£«3H2O(g)””¦¤H£½a kJ”¤mol£1£¬ŌŚŅ»¶ØŃ¹ĒæĻĀ£¬²āµĆøĆ·“Ó¦µÄŹµŃ鏿¾ŻČē±ķĖłŹ¾”£Ēėøł¾Ż±ķÖŠŹż¾Ż»Ų“šĻĀĮŠĪŹĢā”£
CH3CH2OH(g)£«3H2O(g)””¦¤H£½a kJ”¤mol£1£¬ŌŚŅ»¶ØŃ¹ĒæĻĀ£¬²āµĆøĆ·“Ó¦µÄŹµŃ鏿¾ŻČē±ķĖłŹ¾”£Ēėøł¾Ż±ķÖŠŹż¾Ż»Ų“šĻĀĮŠĪŹĢā”£
n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
1.5 | 45 | 33 | 20 | 12 |
2 | 60 | 43 | 28 | 15 |
3 | 83 | 62 | 37 | 22 |
¢ŁÉĻŹö·“Ó¦µÄa________0(Ģī”°“óÓŚ”±»ņ”°Š”ÓŚ”±)”£
¢ŚŗćĪĀĻĀ£¬Ļņ·“Ó¦ĢåĻµÖŠ¼ÓČė¹ĢĢå“߻ƼĮ£¬Ōņ·“Ó¦²śÉśµÄČČĮæ________(Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±)”£
¢ŪŌö“ó![]() µÄÖµ£¬ŌņÉś³ÉŅŅ“¼µÄĪļÖŹµÄĮæ________(Ģī”°Ōö“ó”±”°¼õŠ””±”°²»±ä”±»ņ”°²»ÄÜČ·¶Ø”±)”£
µÄÖµ£¬ŌņÉś³ÉŅŅ“¼µÄĪļÖŹµÄĮæ________(Ģī”°Ōö“ó”±”°¼õŠ””±”°²»±ä”±»ņ”°²»ÄÜČ·¶Ø”±)”£
”¾“š°ø”æ 0.25 mol”¤L£1”¤min£1 B E F B C Š”ÓŚ ²»±ä ²»ÄÜČ·¶Ø
”¾½āĪö”æ(1) ¢Ł“Ó·“Ó¦æŖŹ¼µ½3minŹ±£¬V(CO2)=(1-0.5)/2”Į3=1/12 mol”¤L£1”¤min£1 £¬øł¾Ż·“Ó¦·½³ĢŹ½£ŗCO2+3H2 ![]() CH3OH(g)+H2O(g)£¬»Æѧ¼ĘĮæŹżÖ®±ČµČÓŚ»Æѧ·“Ó¦ĖŁĀŹÖ®±Č£¬ŌņV(H2)=0.25 mol”¤L£1”¤min£1£»ÕżČ·“š°ø£ŗ0.25 mol”¤L£1”¤min£1”£
CH3OH(g)+H2O(g)£¬»Æѧ¼ĘĮæŹżÖ®±ČµČÓŚ»Æѧ·“Ó¦ĖŁĀŹÖ®±Č£¬ŌņV(H2)=0.25 mol”¤L£1”¤min£1£»ÕżČ·“š°ø£ŗ0.25 mol”¤L£1”¤min£1”£
¢ŚŌŚŌČŻĘ÷ÖŠŌŁ³äČė1molCO2£¬CO2µÄ×ÜĪļÖŹµÄĮæŌŚŌö¼Ó,ĖäČ»Ę½ŗāŌŚÕżĻņŅʶÆ,øł¾ŻĄÕĻÄĢŲĮŠŌĄķæÉŅŌÖŖµĄ, CO2µÄ×Ŗ»ÆĀŹ¼õŠ”£¬A“ķĪó£»ŌŚŌČŻĘ÷ÖŠŌŁ³äČė1molH2£¬Ę½ŗāÓŅŅĘ£¬CO2µÄ×Ŗ»ÆĀŹŌö“ó£¬BÕżČ·£»ŌŚŌČŻĘ÷ÖŠ³äČė1molHe£¬¶ŌĘ½ŗāƻӊӰĻģ£¬CO2µÄ×Ŗ»ÆĀŹ²»±ä£¬C“ķĪó£»Ź¹ÓĆøüÓŠŠ§µÄ“߻ƼĮ£¬Ö»ÄܼÓæģ·“Ó¦ĖŁĀŹ£¬Ę½ŗā²»ŅĘ¶Æ£¬CO2µÄ×Ŗ»ÆĀŹ²»±ä£¬D“ķĪó£»ĖõŠ”ČŻĘ÷µÄČŻ»ż£¬Ļąµ±ÓŚ¼ÓŃ¹£¬Ę½ŗāÓŅŅĘ£¬CO2µÄ×Ŗ»ÆĀŹŌö“ó£¬EÕżČ·£»½«Ė®ÕōĘų“ÓĢåĻµÖŠ·ÖĄė³ö£¬¼õŠ”ĮĖĖ®ÕōĘųµÄÅØ¶Č£¬Ę½ŗāÓŅŅĘ£¬CO2µÄ×Ŗ»ÆĀŹŌö“ó£¬FÕżČ·£»ÕżČ·“š°ø£ŗB E F”£
¢Ū»Æѧ¼ĘĮæŹżÖ®±ČµČÓŚ»Æѧ·“Ó¦ĖŁĀŹÖ®±Č£¬v(H2)=3v(CO2)£¬µ«Ć»ÓŠÖøĆ÷ÕżÄę·“Ó¦·½Ļņ£¬ĪŽ·ØÅŠ¶Ø·“Ó¦ŅŃ“ļĘ½ŗāדĢ¬£¬A“ķĪó£»øĆ·“Ó¦ŹĒŅ»øö·“Ó¦Ē°ŗóĘųĢåĢå»ż±äµÄ»Æѧ·“Ó¦£¬øĆ·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬ČŻĘ÷ÖŠĘųĢåŃ¹Ēæ²»±ä£¬BÕżČ·£»»Æѧ¼ĘĮæŹżÖ®±ČµČÓŚ»Æѧ·“Ó¦ĖŁĀŹÖ®±Č£¬ĒŅ±ķĆ÷ÕżÄę·“Ó¦·½Ļņ£¬æÉŅŌÅŠ¶Ø·“Ó¦ŅŃ“ļĘ½ŗāדĢ¬£¬CÕżČ·£»·“Ó¦Ē°ŗóĘųĢåµÄ×ÜÖŹĮæ²»±ä£¬ČŻĘ÷µÄĢå»ż²»±ä£¬ĪŽĀŪøĆ·“Ó¦ŹĒ·ń“ļµ½Ę½ŗāדĢ¬£¬ČŻĘ÷ÄŚĘųĢåĆܶȏ¼ÖÕ²»±ä£¬D“ķĪó£»ÕżČ·Ń”ĻīB C”£
(2)¢ŁÓÉĶ¼±ķ·ÖĪöÅŠ¶Ļ£¬ĖęĪĀ¶ČÉżøߣ¬¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹ¼õŠ”£¬ĖµĆ÷Ę½ŗāÄęĻņ½ųŠŠ£¬ÄęĻņŹĒĪüČČ·“Ó¦£¬ÕżĻņŹĒ·ÅČČ·“Ó¦£¬aŠ”ÓŚ0£»ÕżČ·“š°ø£ŗŠ”ÓŚ”£
¢Ś“߻ƼĮ¶Ō»ÆŃ§Ę½ŗāƻӊӰĻģ,ĖłŅŌ¼ÓČė“߻ƼĮ,Ę½ŗā²»ŅʶÆ,·“Ó¦·“Ó¦ČČ²»±ä£¬ÕżČ·“š°ø£ŗ²»±ä”£
(3)ĒāĘųŗĶ¶žŃõ»ÆĢ¼ĪļÖŹµÄĮæ±ČÖµŌö“ó,æÉŅŌŹĒŌö¼ÓĒāĘų,Ņ²æÉÄÜĪŖ¼õŠ”¶žŃõ»ÆĢ¼,ĖłŅŌ¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹŌö“󣬵«Éś³ÉµÄŅŅ“¼µÄĪļÖŹµÄĮæ²»Ņ»¶ØŌö“ó»ņ¼õŠ”£¬ÕżČ·“š°ø£ŗ²»ÄÜČ·¶Ø”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æX”¢Y”¢Z”¢Q”¢W”¢RĮłÖÖ¶ĢÖÜĘŚŌŖĖŲŌ×ÓŠņŹżŅĄ“ĪŌö“󔣻ÆŗĻĪļ¼×Ė׳ĘæĮŠŌÄĘ£¬ÓÉX”¢Z”¢QČżÖÖŌŖĖŲ×é³É”£Ņ½Ń§ÖŠ³£ÓĆQRČÜŅŗÅäÖĘÉśĄķŃĪĖ®”£»ÆŗĻĪļŅŅÓÉX”¢RĮ½ÖÖŌŖĖŲ×é³É”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
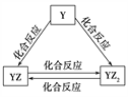
(1)QµÄĄė×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ____________________”£
(2)YŌŖĖŲµÄµ„ÖŹ¼°Ęä»ÆŗĻĪļÄÜ·¢ÉśČēÉĻĶ¼ĖłŹ¾µÄ×Ŗ»Æ£¬ŌņYŌŖĖŲĪŖ___(ĢīŌŖĖŲ·ūŗÅ)”£ŌŚ¼×ČÜŅŗÖŠĶØČė×ćĮæYZ2ĘųĢ壬Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ________________________”£
(3)WµÄµ„ÖŹ¼ČÄÜÓė¼×ČÜŅŗ·“Ó¦£¬ÓÖÄÜÓėŅŅČÜŅŗ·“Ó¦”£³£ĪĀĻĀ£¬½«WµÄµ„ÖŹŗĶ¼×ČÜŅŗ»ģŗĻ£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ___________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲŹµŃé×°ÖĆ½ųŠŠµÄĻąÓ¦ŹµŃ飬²»ÄÜ“ļµ½ŹµŃéÄæµÄµÄŹĒ
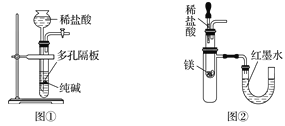
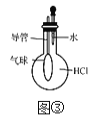
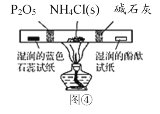
A. ÓĆĶ¼¢ŁĖłŹ¾×°ÖĆÖĘȔɣĮæ“æ¾»µÄCO2ĘųĢå
B. ÓĆĶ¼¢ŚĖłŹ¾×°ÖĆŃéÖ¤Ć¾ŗĶŃĪĖį·“Ó¦µÄČČŠ§Ó¦
C. ÓĆĶ¼¢ŪĖłŹ¾×°ÖĆŃéÖ¤HClĘųĢåŅ×ČÜÓŚĖ®
D. ÓĆĶ¼¢ÜĖłŹ¾×°ÖĆ¼ģŃéNH4Cl·Ö½ā²śÉśµÄĘųĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠČČ»Æѧ·½³ĢŹ½£¬ÕżČ·µÄŹĒ(””””)
A. ¼×ĶéµÄČ¼ÉÕČȦ¤H£½£890.3 kJ”¤mol£1£¬Ōņ¼×ĶéČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ CH4(g)£«2O2(g)===CO2(g)£«2H2O(g)””¦¤H£½£890.3 kJ”¤mol£1
B. 500 ”ę”¢30 MPaĻĀ£¬½«0.5 mol N2(g)ŗĶ1.5 mol H2(g)ÖĆÓŚĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ӧɜ³ÉNH3(g)£¬·ÅČČ19.3 kJ£¬ĘäČČ»Æѧ·½³ĢŹ½ĪŖN2(g)£«3H2(g)![]() 2NH3(g)””¦¤H£½£38.6 kJ”¤mol£1
2NH3(g)””¦¤H£½£38.6 kJ”¤mol£1
C. HClŗĶNaOH·“Ó¦µÄÖŠŗĶČȦ¤H£½£57.3 kJ”¤mol£1£¬ŌņH2SO4ŗĶCa(OH)2·“Ó¦µÄÖŠŗĶČȦ¤H£½2”Į(£57.3)kJ”¤mol£1
D. ŌŚ101 kPaŹ±£¬2 g H2ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®£¬·Å³ö285.8 kJČČĮ棬ĒāĘųČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½±ķŹ¾ĪŖ2H2(g)£«O2(g)===2H2O(l)””¦¤H£½£571.6 kJ”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
A. ŗ¬0.1 mol Na2O2µÄ¾§ĢåÖŠŃōĄė×ÓÓėŅõĄė×Ó×ÜŹżĪŖ0.4NA
B. 46 g NO2ŗĶN2O4µÄ»ģŗĻĘųĢåÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖ2NA
C. 1 mol FeÓėŅ»¶ØĮæĻõĖįĒ”ŗĆĶźČ«·“Ó¦Ź±£¬×ŖŅʵē×ÓŹżŅ»¶ØĪŖ3NA
D. 1 mol CH4Óė¹żĮæĀČĘų·¢ÉśČ”“ś·“Ó¦£¬Éś³ÉCH3ClĘųĢåµÄĢå»żŌ¼ĪŖ22.4 L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§ĄūÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠĢśøśĖ®ÕōĘų·“Ó¦µÄŹµŃ飬²¢¼ĢŠųŃŠ¾æĢś¼°Ęä»ÆŗĻĪļµÄ²æ·ÖŠŌÖŹ”£
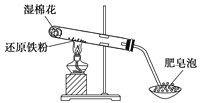
£Ø1£©ŹŌ¹ÜÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_______________________________”£
£Ø2£©øĆĶ¬Ń§ÓūČ·¶Ø·“Ó¦Ņ»¶ĪŹ±¼äŗóŹŌ¹ÜÖŠ¹ĢĢåĪļÖŹµÄ³É·Ö£¬Éč¼ĘĮĖČēĻĀ·½°ø£ŗ
¢Ł“żŹŌ¹ÜĄäČ“£¬Č”ĘäÖŠ¹ĢĢåÉŁŠķČÜÓŚĻ”ŃĪĖįµĆČÜŅŗB£»
¢ŚČ”ÉŁĮæČÜŅŗBµĪ¼ÓKSCNČÜŅŗ£¬ČōČÜŅŗ±äŗģ£¬ŌņŹŌ¹ÜÖŠ¹ĢĢåŹĒ________(Ö»ÓŠŅ»øöŃ”Ļī·ūŗĻĢāŅā)£¬ČōČÜŅŗĪ“±äŗģ£¬ŌņŹŌ¹ÜÖŠ¹ĢĢåŹĒ________(Ö»ÓŠŅ»øöŃ”Ļī·ūŗĻĢāŅā)”£
A£®Ņ»¶ØÓŠFe3O4£¬æÉÄÜÓŠFe
B£®Ö»ÓŠFe(OH)3
C£®Ņ»¶ØÓŠFe3O4ŗĶFe
D£®Ņ»¶ØÓŠFe(OH)3£¬æÉÄÜÓŠFe
E£®Ö»ÓŠFe3O4
£Ø3£©øĆĶ¬Ń§°“ÉĻŹö·½°ø½ųŠŠĮĖŹµŃ飬ČÜŅŗĪ“±äŗģÉ«£¬ŌŅņŹĒ£ŗ __________________________(ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾)”£
£Ø4£©øĆĶ¬Ń§ĀķÉĻĮķȔɣĮæČÜŅŗB£¬Ź¹ĘäøśNaOHČÜŅŗ·“Ó¦”£Čō°“ÓŅĶ¼ĖłŹ¾µÄ²Ł×÷£¬æɹŪ²ģµ½Éś³É°×É«³Įµķ£¬ŃøĖŁ±ä³É»ŅĀĢÉ«£¬×īŗó±ä³ÉŗģŗÖÉ«µÄĻÖĻó£¬ĒėŠ“³öÓėÉĻŹöĻÖĻóĻą¹Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½__________________________________________________£¬______________________________________”£
£Ø5£©Ņ»¶ĪŹ±¼äŗó£¬øĆĶ¬Ń§·¢ĻÖ(3)ÖŠĪ“±äŗģµÄČÜŅŗ±ä³ÉŗģÉ«”£ÓÉ“ĖæÉÖŖ£¬ŹµŃéŹŅFeCl2ČÜŅŗŠčĻÖÓĆĻÖÅäµÄŌŅņŹĒ___________________________________£¬²¢ĒŅÅäÖĘŹ±Ó¦¼ÓČėÉŁĮæ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻµČµē×ÓŌĄķÅŠ¶Ļ£¬ĻĀĮŠĖµ·ØÖŠ“ķĪóµÄŹĒ(””””)
A. B3N3H6£Ø±ČĄżÄ£ŠĶČēĶ¼£©·Ö×ÓÖŠĖłÓŠŌ×Ó¾łŌŚĶ¬Ņ»Ę½ĆęÉĻ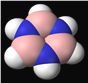
B. B3N3H6·Ö×ÓÖŠ“ęŌŚĖ«¼ü£¬æÉ·¢Éś¼Ó³É·“Ó¦
C. H3O£«ŗĶNH3ŹĒµČµē×ÓĢ壬¾łĪŖČż½Ē׶ŠĶ
D. CH4ŗĶNH4+ŹĒµČµē×ÓĢ壬¾łĪŖÕżĖÄĆęĢå½į¹¹
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗ»¹ŌŠŌHSO3”Ŗ>I”Ŗ£¬Ńõ»ÆŠŌIO3”Ŗ>I2”£ŌŚŗ¬3molNaHSO3µÄČÜŅŗÖŠÖšµĪ¼ÓČėKIO3ČÜŅŗ”£¼ÓČėKIO3ŗĶĪö³öI2µÄĪļÖŹµÄĮæµÄ¹ŲĻµĒśĻßČēĻĀĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
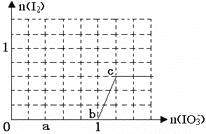
A. 0”«a¼ä·¢Éś·“Ó¦£ŗ3HSO3”Ŗ+IO3”Ŗ=3SO42-+I”Ŗ+3H+
B. a”«b¼ä¹²ĻūŗÄNaHSO3µÄĪļÖŹµÄĮæĪŖ1.8mol
C. b”«c¼ä·“Ó¦£ŗI2½öŹĒŃõ»Æ²śĪļ
D. µ±ČÜŅŗÖŠI-ÓėI2µÄĪļÖŹµÄĮæÖ®±ČĪŖ5”Ć3Ź±£¬¼ÓČėµÄKIO3ĪŖ1.1mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§½ųŠŠÓŠ¹ŲĶ”¢ĻõĖį”¢ĮņĖį»ÆѧŠŌÖŹµÄŹµŃ飬ŹµŃé¹ż³ĢČēĶ¼ĖłŹ¾£ŗ
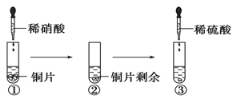
¢Ł”¢¢Ū¾ł¹Ū²ģµ½ŹµŃéĻÖĻó£ŗČÜŅŗ³ŹĄ¶É«£¬ŹŌ¹ÜæŚÓŠŗģ×ŲÉ«ĘųĢå²śÉś”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. ¢ŁŹŌ¹ÜæŚÓŠŗģ×ŲÉ«ĘųĢå²śÉś£¬ŌŅņŹĒĻõĖį±»»¹ŌĪŖNO2
B. ÓÉ¢ŪµÄĻÖĻóæÉµĆ³ö½įĀŪ£ŗCuæÉÓėĻ”ĮņĖį·“Ó¦
C. ¢ŪÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ3Cu£«2NO3-+8H+ === 3Cu2+£«2NO”ü£«4H2O
D. ¢ŪÖŠæÉÄܲśÉśSO2
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com