
����Ŀ��ͬһ�������ڵ�A��B��C����Ԫ�أ����Ƕ�����Ԫ�أ�A�����������Ļ�ѧʽ��A2O��11.6 g B����������ǡ������200 mL 2 mol/L������ȫ��Ӧ��Bԭ�Ӻ�������������������ȡ��ش��������⣺
��1��B�����ԭ�������Ƕ��٣�ԭ�������Ƕ��٣�_____________
��2��A��C����ʲôԪ�أ�_____________
��3��A��B��C�ĵ��ʸ�1 mol�ֱ���������ϡ���ᷴӦ������H2��������һ�ֵ��ʣ��õ��ʲ���H2������ڱ�״�����Ƕ���?_______________
���𰸡�24��12 A��Na��C��Al Al��33.6L
��������
A�����������Ļ�ѧʽΪA2O��A�ԣ�1�ۣ�Aλ��IA�壬B�����������������ᷴӦ��A��B��CΪ����Ԫ��ͬ����Ԫ�أ�Bλ�ڢ�A�壬����������ΪB(OH)2����������������BΪMg����AΪNa��CΪAl���ݴ˷�����
A�����������Ļ�ѧʽΪA2O��A�ԣ�1�ۣ�Aλ��IA�壬B�����������������ᷴӦ��A��B��CΪ����Ԫ��ͬ����Ԫ�أ�Bλ����A�壬����������ΪB(OH)2��
(1)������������ʵ���200��10��3L��2mol��L��1=0.4mol����B(OH)2��Ħ������ΪMg��mol��1�� 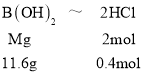
M��58��B�����ԭ��������58��2��(16��1)��24����Bԭ�Ӻ�������������������ȣ�����B��ԭ������Ϊ12��BΪþԪ�أ�
(2)�������֪��AΪNa��CΪAl��
(3)���ݵ�ʧ������Ŀ�غ㣬�ֱ�ó�n(Na)��1=n(H2)��2��n(Mg)��2=n(H2)��2��n(Al)��3= n(H2)��2����Ϊ���ֽ����������ʵ�����ȣ���˲���H2���Ľ����� Al��1molAl����H2�����ʵ���Ϊ1.5mol������״���£�V(H2)=1.5mol��22.4L��mol��1=33.6L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӵ������������ѧ�ң�1776.08.09-1856.07.09��������ҵ����ʦ��24�������������ʮ���ڷܣ��ճ�һ����ѧ��ʦ��Ϊ�˼����������ǰ�1 molij���������������е����Ӹ�������Ϊ�����ӵ���������N![]() ��ʾ������˵�����ʾ�в���ȷ����
��ʾ������˵�����ʾ�в���ȷ����

A.��ѧ�Ϲ涨���а����ӵ����������ӵ��κ��������嶼Ϊ1 mol
B.��K37ClO3+6H35Cl��Ũ��=KCl+3Cl2��+3H2O��Ӧ�У�����212���������ɣ���Ӧ�е���ת�Ƶ���ĿΪ5NA
C.60 �˵�����������ǻ������ȼ������2NA��O2
D.6.02��1023mol-1 ���������ӵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ֻ�ѧ���ļ��ܺ��Ȼ�ѧ����ʽ���£�
��ѧ�� | H��N | N��N | Cl��Cl | N | H��Cl |
����/(kJ��mol��1) | 391 | 193 | 243 | 946 | 432 |
N2H4(g)��2Cl2(g)=N2(g)��4HCl(g) ��H�������ƶ���ȷ���ǣ� ��
A.H(g)��Cl(g)=HCl(g) ��H����432kJ��mol��1
B.����1molCl��Cl�����������ȶ���1molN![]() N����703kJ
N����703kJ
C.������Ӧ�У���H����431kJ��mol��1
D.������Ӧ�У����Ѽ��Լ��ͷǼ��Լ���ֻ�γɼ��Լ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬ�¶��£�����������ĵ���ƽ�ⳣ���������ж���ȷ����![]()
�� | HX | HY | HZ |
|
|
|
|
A.�������ǿ����ϵ�� ![]()
B.��Ӧ ![]() �ܹ�����
�ܹ�����
C.��ͬ�¶��£�![]() ��NaX��NaY��NaZ��Һ��NaZ��ҺpH���
��NaX��NaY��NaZ��Һ��NaZ��ҺpH���
D.��ͬ�¶��£�![]() ��Һ�ĵ��볣������
��Һ�ĵ��볣������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(N2H4)�ڲ�ͬ�����·ֽ���ﲻͬ��200��ʱ��Cu����ֽ�Ļ�����ͼ����֪200��ʱ����Ӧ��3N2H4(g)=N2(g)+4NH3(g) ��H1=-32.9 kJ��mol-1��Ӧ��N2H4(g)+H2(g)2NH3(g)��H2=-41.8 kJ��mol-1

����˵������ȷ����()
A. ͼ��ʾ���̢��Ƿ��ȷ�Ӧ
B. ��Ӧ�����������ʾ��ͼ��ͼ��ʾ
C. �Ͽ�3 mol N2H4(g)�Ļ�ѧ�����յ����������γ�1 molN2(g)��4 mol NH3(g)�Ļ�ѧ���ͷŵ�����
D. 200��ʱ���·ֽ����ɵ������������Ȼ�ѧ����ʽΪN2H4(g)=N2(g)+2H2(g)��H=+50.7 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�����ڣ������뻯ѧ�йص�˵������ȷ���ǣ� ��
A.�����Ƽ�Ĺ��չ�����Ӧ���������ܽ�ȵIJ���
B.��ҵ����������ʯ����Ϊԭ���Ʊ�Ư��
C.���ʹ賣�������ά�IJ��ϣ������İ뵼��������һ����ϵ
D.��ѹ�ƵƷ����Ļƹ����Զ��������ǿ��������·��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ú�﮷�������Ҫ����Ԫ�صĺ�����Li 3.50% Ni 6.55% Ca 6.41% Mg 13.24%)�Ʊ�Li2CO3,�������Ʊ�﮵�ص���������LiFePO4�����ֹ����������£�
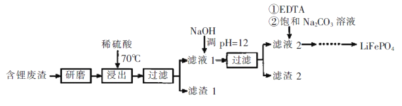
���ϣ�i��Һ1����Һ2�в�������Ũ�ȣ�g��L��1��
Li�� | Ni2�� | Ca2�� | Mg2�� | |
��Һ1 | 22.72 | 20.68 | 0.36 | 60.18 |
��Һ2 | 21.94 | 7.7��10��3 | 0.08 | 0.78��10��3 |
ii��EDTA�ܺ�ijЩ���۽��������γ��ȶ���ˮ���������
iii��ijЩ���ʵ��ܽ�ȣ�S��
T/�� | 20 | 40 | 60 | 80 | 100 |
S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
S(Li2SO4)/g | 34.7 | 33.6 | 32.7 | 31.7 | 30.9 |
I.�Ʊ�Li2CO3��Ʒ
��1������������Ϊ�ӿ컯ѧ��Ӧ���ʶ���ȡ�Ĵ�ʩ��____��
��2������2����Ҫ�ɷ���____��
��3������Һ2���ȼ���EDTA,�ټ��뱥��Na2C03��Һ,90���ַ�Ӧ��������� Li2CO3��Ʒ�IJ�����_______��
��4������lkg���3.50%�ķ�����﮵Ľ�����Ϊa��Li+ת��ΪLi2CO3��ת����Ϊb�����Ʒ�к�Li2CO3��������________g����Ħ������:Li2CO3 74 g.mol4)
II.����Li2CO3��Ʒ
��5����Li2CO3ת��ΪLiHCO3���ø�Ĥ�����LiHCO31��Һ�Ʊ��ߴ��ȵ�LiOH,��ת���õ�ؼ�Li2CO3�����ԭ����ͼ��ʾ�������ĵ缫��Ӧʽ��____,�ó�ʹ����_________(���������������������ӽ���Ĥ��
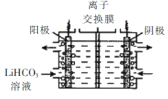
��.�Ʊ� LiFePO4
��6������ؼ�Li2CO3��C��FePO4�����·�Ӧ������LiFePO4��һ�ֿ�ȼ������,�÷�Ӧ�Ļ�ѧ����ʽ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г��������¼ס��ҡ���������Һ����Ϊ0.1 mol��L��1��NaOH��Һ����Ϊ0.1 mol��L��1��HCl��Һ����Ϊ0.1 mol��L��1��CH3COOH��Һ���Իش��������⣺
(1)����Һ��pH��________��
(2)����Һ����ˮ�������H��Ũ��Ϊ________mol��L��1��
(3)�����£���ˮϡ��0.1 mol��L��1��CH3COOH��Һʱ�����и�����ˮ�������Ӷ��������________(�����)��
��n(H��) ��c(H��) ��![]() ��c(OH��)
��c(OH��)
(4)ijͬѧ�ü���Һ������Һ�ֱ�ζ�20.00 mL����Һ��20.00 mL����Һ���õ���ͼ��ʾ�������ζ����ߣ���ش��й����⣺
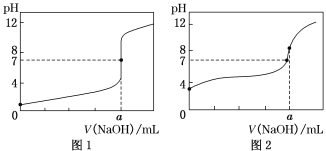
������Һ�ζ�����Һ��������_______(����ͼ1������ͼ2��)���ߡ�
���ü���Һ�ζ�����Һʵ���У�ָʾ��Ӧѡ��________���ζ��ﵽ�յ������Ϊ��____________���ζ�ǰδ�ñ�Һ��ϴ�ζ��ܣ������ɵζ����______ (��ƫ�ߡ�ƫ�ͻ���Ӱ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С�齫��ͼ��ʾװ�ð�һ��˳�����ӣ���ʵ��������ȡһ������![]() ��ͨ�����������ַ�Ӧ
��ͨ�����������ַ�Ӧ![]() ����ش��������⣺
����ش��������⣺
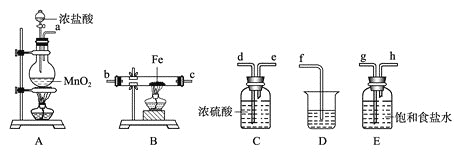
![]() �з�����Ӧ�Ļ�ѧ����ʽΪ_____________________��
�з�����Ӧ�Ļ�ѧ����ʽΪ_____________________��
![]() ��װ�õ���ȷ����˳��Ϊ
��װ�õ���ȷ����˳��Ϊ![]() ��дװ�ô���
��дװ�ô���![]() ____
____![]() ____
____![]() ____
____![]() ��
��
![]() д��װ��D�з�Ӧ�����ӷ���ʽ_____________________��
д��װ��D�з�Ӧ�����ӷ���ʽ_____________________��
![]() ��Ӧ�������Լ���B���������к���
��Ӧ�������Լ���B���������к���![]() ���Լ���_______
���Լ���_______![]() ��д�Լ�����
��д�Լ�����![]() ��
��
![]() ��С��������ͼ��ʾװ���ռ�β������������������������
��С��������ͼ��ʾװ���ռ�β������������������������
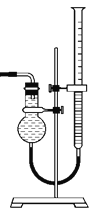
![]() ��ͼ����ʾ����װ���ɸ���ܡ��齺�ܺ�
��ͼ����ʾ����װ���ɸ���ܡ��齺�ܺ�![]() �ζ��ܸ������װ���ɣ��˴����õζ�����_____________
�ζ��ܸ������װ���ɣ��˴����õζ�����_____________![]() ������ʽ��������ʽ��
������ʽ��������ʽ��![]() �ζ��ܡ�
�ζ��ܡ�
![]() Ϊ��߲�����ȷ�ԣ���ͼװ���е�Һ�����___________��
Ϊ��߲�����ȷ�ԣ���ͼװ���е�Һ�����___________��
![]() �����ʼ����ʱ������ȷ��������ʱ�����ұߵζ���Һ�棬�ᵼ��������������_______
�����ʼ����ʱ������ȷ��������ʱ�����ұߵζ���Һ�棬�ᵼ��������������_______![]() ����ƫ��������ƫС��������Ӱ����
����ƫ��������ƫС��������Ӱ����![]() ��
��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com