
| A. | 卤素有单质存在于自然界中 | |
| B. | 随核电荷数增加,单质熔沸点升高 | |
| C. | 随核电荷数增加,单质氧化性增强 | |
| D. | 单质与水反应,均可用通式X2+H2O═HX+HXO表示 |
分析 A.卤素单质性质很活泼,极易和其它物质反应;
B.随着核电荷数增大,单质的熔沸点升高;
C.随着核电荷数增大,单质的氧化性逐渐减弱;
D.氟气与水反应生成氧气.
解答 解:A.卤素原子最外层有7个电子,极易得电子生成8电子稳定结构,所以卤素单质性质很活泼,极易和其它物质反应,导致卤素只以化合态存在于自然界中,故A错误;
B.随着核电荷数增大,单质的相对分子质量最大,分子间作用力最大,单质的熔沸点升高,故B正确;
C.随着核电荷数增大,卤素原子对最外层电子的吸引能力逐渐减小,导致单质的氧化性逐渐减弱,故C错误;
D.氟气与水反应生成氧气,其它单质与水反应,均可用通式X2+H2O═HX+HXO表示,故D错误;
故选B.
点评 本题考查了第VIIA族元素性质的相似性及递变性,根据元素周期律来分析解答即可,知道结构和性质的关系,题目难度不大.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ①>②>③>④>⑤ | B. | ③>④>⑤>②>① | C. | ⑤>④>③>②>① | D. | ②>①>⑤>④>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
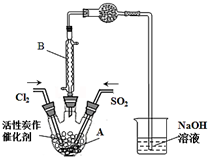 某学习小组依据反应:SO2(g)+Cl2(g?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.
某学习小组依据反应:SO2(g)+Cl2(g?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.| SO2Cl2 | Cl2 | SO2 | |
| 熔点/℃ | -54.1 | -101 | -72.4 |
| 沸点/℃ | 69.1 | -34.6 | -10 |
| 性质 | 遇水发生剧烈 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干冰、冰、金属钠 | B. | 二氧化硅、食盐、硫 | ||
| C. | 金刚石、碘、氧化钙 | D. | HF、HCl、HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
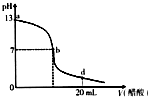
| A. | 该氢氧化钠溶液的物质的量浓度为0.1 mol/L | |
| B. | 在b点,c(Na+)=c(CH3COO-) | |
| C. | 在d点,溶液中所有离子浓度由大到小的顺序为c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| D. | 氢氧化钠溶液与醋酸溶液恰好完全反应的点位于曲线b、d间的某点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
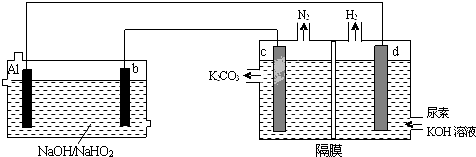
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KNO3 | B. | CO(NH2)2 | C. | Ca(H2PO4)2 | D. | (NH4)2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com