
| ČõĖį»ÆѧŹ½ | CH3COOH | HCN | H2CO3 |
| µēĄėĘ½ŗā ³£Źż(25 ”ę) | 1.8”Įl0£5 | 4.9”Įl0£10 | K1£½4.3”Įl0£7 K2£½5.6”Įl0£11 |


 ¼ĘĖćøߏÖĻµĮŠ“š°ø
¼ĘĖćøߏÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®1 mol”¤L-1µÄ¼×ĖįČÜŅŗµÄc(H+)ĪŖ1”Į10-2 mol”¤L-1 |
| B£®¼×ĖįÄÜÓėĖ®ŅŌČĪŅā±Č»„ČÜ |
| C£®10 mL 1 mol”¤L-1µÄ¼×ĖįČÜŅŗĒ”ŗĆÓė10 mL 1 mol”¤L-1µÄNaOHČÜŅŗĶźČ«·“Ó¦ |
| D£®µĪČėŹÆČļŹŌŅŗĻŌŗģÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®µēĄė³£Źż£ŗK(HCN) £¼Ka2 (H2CO3) |
| B£®ÅØ¶Č¾łĪŖ0.1mol”¤L-1µÄNaCNŗĶNaHCO3ČÜŅŗµÄpH£ŗNaCN £¼NaHCO3 |
| C£®ÅØ¶Č¾łĪŖ0.1mol”¤L-1µÄNaCNŗĶNa2CO3ČÜŅŗÖŠ£¬ŅõĄė×Ó×ÜÅضČĻąµČ |
| D£®pH¾łĪŖ10µÄ Na2CO3ČÜŅŗ”¢NaCNČÜŅŗÖŠ£¬Ė®µēĄė²śÉśµÄc£ØOH-£©ĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®NaCl(s) | B£®CaCO3(s) | C£®H2O | D£®NaOH(s) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| | ¢Ł | ¢Ś | ¢Ū | ¢Ü | ¢Ż |
| ČÜŅŗ | °±Ė® | ĒāŃõ»ÆÄĘ | “×Ėį | ŃĪĖį | “×ĖįÄĘ |
| pH | 11 | 11 | 3 | 3 | 8£®3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

A£®ŌŚĻąĶ¬ĪĀ¶ČĻĀ£¬ £¾ £¾ £¾ £¾ |
B£®ŹŅĪĀŹ±£¬ČōŌŚNaZČÜŅŗÖŠ¼ÓĖ®£¬Ōņ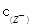 £Æ £Æ ”¤ ”¤ µÄ±ČÖµ±äŠ”£¬Čō¼ÓÉŁĮæŃĪĖį£¬Ōņ±ČÖµ±ä“ó µÄ±ČÖµ±äŠ”£¬Čō¼ÓÉŁĮæŃĪĖį£¬Ōņ±ČÖµ±ä“ó |
C£®µČĪļÖŹµÄĮæÅØ¶ČµÄNaX”¢NaYŗĶNaZµÄ»ģŗĻČÜŅŗ£¬Ōņ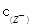 £¼ £¼ £¼ £¼ |
D£®ŌŚĻąĶ¬ĪĀ¶Č£¬“ÓHXµÄŹż¾ŻæÉŅŌĖµĆ÷£ŗČõµē½āÖŹČÜŅŗÅضČŌ½µĶ£¬µēĄė¶ČŌ½“ó£¬ĒŅ £¾ £¾ £¾ £¾ £½0.01 £½0.01 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com