
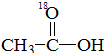 在水溶液中存在平衡:
在水溶液中存在平衡: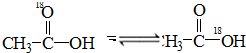 当
当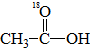 与 CH3CH2OH发生酯化反应时,不可能生成的产物是( )
与 CH3CH2OH发生酯化反应时,不可能生成的产物是( )| A. | 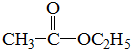 | B. | 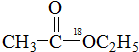 | C. | H2O | D. | H218O |
分析 羧酸跟醇的酯化反应是可逆的,羧酸跟醇的反应过程一般是:羧酸分子中的羟基与醇分子中羟基的氢原子结合成水,其余部分互相结合成酯,即酸去羟基醇去羟基氢.可用示踪原子证实;再根据CH3C18OOH?CH3CO18OH进行分析可能生成的产物,以此解答该题.
解答 解:乙酸与乙醇反应乙酸提供羟基,醇提供羟基氢原子,结合生成水,其余部分互相结合成酯,乙酸与乙醇反应方程式为:CH3C18OOH+CH3CH2OH?CH3C18OOC2H5+H2O;由于CH3C18OOH在水溶液中存在平衡:CH3C18OOH?CH3CO18OH,所以还可能发生反应:CH3CO18OH+CH3CH2OH?CH3COOC2H5+H218O,所以反应生成产物可能为:CH3C18OOC2H5、H2O、CH3COOC2H5、H218O,不可能生成CH3CO18OC2H5,
故选B.
点评 本题考查有机物的结构和性质,侧重考查酯化反应原理、化学反应的可能性,题目难度中等,注意明确酯化反应的原理,充分理解应用题中信息:CH3C18OOH?CH3CO18OH是解题关键.


科目:高中化学 来源: 题型:解答题
 硼及其化合物在工业上有许多用途.工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5•H2O和Fe3O4.
硼及其化合物在工业上有许多用途.工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5•H2O和Fe3O4.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示在密封容器中,一部分装入2.3g金属钠,另一部分装入HgO,同时加热两部分,若加热后容器内的空气成分未变,那么装入容器中的HgO是( )
如图所示在密封容器中,一部分装入2.3g金属钠,另一部分装入HgO,同时加热两部分,若加热后容器内的空气成分未变,那么装入容器中的HgO是( )| A. | 21.6 g | B. | 20.0g | C. | 1.6 g | D. | 10.8 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10种 | B. | 12种 | C. | 14种 | D. | 16种 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用过滤的方法可以分离出溶液与胶体 | |
| B. | 在江河入海口处易形成沙洲 | |
| C. | 一束平行光线照射蛋白质溶液时从侧面可以看到一束光亮的通路 | |
| D. | 三氯化铁溶液中滴加氢氧化钠溶液出现氢氧化铁的胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减少,其方法是加入氢氧化钠固体 | |
| B. | 常温下,0.4 mol/LHB溶液和0.2 mol/LNaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为: c(B-)>c(H+)>c(Na+)>c(OH-) | |
| C. | 某温度下纯水的c(H+)=1.0×10-6mol/L,在此温度下,将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合(溶液体积变化忽略不计).欲使混合溶液的pH=7,则氢氧化钡溶液与盐酸的体积比为2:9 | |
| D. | pH相等的下列溶液:a.CH3COOK、b.NaHCO3、c.Na2CO3、d.NaOH,其物质的量浓度由小到大顺序为:d<c<a<b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加6.5 g | B. | 减少6.5 g | C. | 减少5.6 g | D. | 增加6.4 g |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com