
��15�֣�����ͭ�ڻ�����ũҵ�����кܹ㷺���ô���ij��ѧ��ȤС��������ϣ������ֲ�ͬ��ԭ����ȡ����ͭ��
��ʽһ��һ�ֺ�ͭ�Ŀ�ʯ�����ȸʯ��ۣ�����ͭ��̬ΪCuCO3��Cu(OH)2��CuSiO3��2H2O������SiO2��FeCO3��Fe2O3��Al2O3�����ʣ��������ֿ�ʯΪԭ����ȡ����ͭ�Ĺ�����������ͼ��
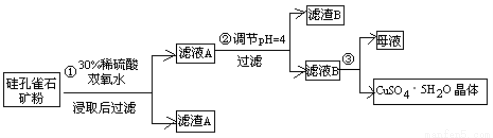
��ش��������⣺
����ɲ������ϡ������CuSiO3��2H2O������Ӧ�Ļ�ѧ����ʽ
CuSiO3��2H2O+H2SO4=CuSO4 +________+H2O��
�Ʋ���ڵ�����ҺpHѡ�õ�����Լ���__________________
A. CuO B. MgO C. FeCO3 D NH3��H2O
���й��������↑ʼ��������ȫ������pH���±���
�������� | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
��ʼ������pH | 3.3 | 1.5 | 6.5 | 4.2 |
������ȫ��pH | 5.2 | 3.7 | 9.7 | 6.7 |
���ϱ���֪������ҺpH=4ʱ��������ȫ��ȥ��������________��
����ҺBͨ������Ũ���������Ũ��Ϊԭ����һ�룩����ȴ�ᾧ���Եõ�CuSO4��5H2O���塣ijͬѧ��Ϊ������������������������������������������ݶԸ�ͬѧ�Ĺ۵��������ۣ���֪�����£�Al2(SO4)3 ������Һ��C(Al3+)=2.25mol��L-1��Ksp[Al(OH)3]=3.2��10-34) ________�����ȷ��������
��ʽ�����Ի�ͭ��Ϊԭ�ϣ���ȡ����ͭ������ͭ�Ĺ���������ʾ��
��.����ͭ����Ҫ�ɷ�ΪCuFeS2����������CaO��MgO��Al2O3������
��.��������װ�ý��е绯ѧ����ʵ�飬����ѡ��ͭ��ۼ�����������������ٽ��裬ʹ����ܽ⡣��������ͨ������������������������
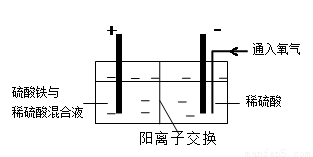
��.һ��ʱ���ȡ��������Һ�������м����л���ȡ����RH��������Ӧ��
2RH���л��ࣩ+ Cu2+��ˮ�ࣩ R2Cu���л��ࣩ+ 2H����ˮ�ࣩ
R2Cu���л��ࣩ+ 2H����ˮ�ࣩ
������л��࣬�����м���һ��Ũ�ȵ����ᣬʹCu2+����������
��.�������ͭ��Һ�Ƶý���ͭ��
��5����ͭ��ۼ��������������ἰ��������Ҫ�������·�Ӧ��
CuFeS2 + 4H�� = Cu2+ + Fe2+ + 2H2S 2Fe3+ + H2S = 2Fe2+ + S��+ 2H��
�������У�������Fe3+��Ũ�Ȼ������ֲ��䣬ԭ����____________________���õ缫��Ӧʽ��ʾ����
��6����������л����м���һ��Ũ�ȵ����ᣬCu2+����������ԭ����_____________ ��
��7��������������0.1mol CuSO4��Һ������ͭ3.2 g����ʱ��Һ������Ũ���ɴ�С��˳���� ____ ��
��15�֣���1��H4SiO4 ��2�֣�
��2��A ��2�֣�
��3��Al3+ ��2�֣�
��4������3�֣�
��5��Fe2+- e��=Fe3+��2�֣�
��6������H+Ũ�ȣ�ʹƽ��2RH(�л���) + Cu2+(ˮ��)  R2Cu(�л���)+ 2H��(ˮ��)�����ƶ���Cu2+����ˮ��������� ��2�֣�
R2Cu(�л���)+ 2H��(ˮ��)�����ƶ���Cu2+����ˮ��������� ��2�֣�
��7�� c(H+)>c(SO42-)>c(Cu2+)>c(OH-)��2�֣�
��������
�����������1�����������غ㶨�ɣ��հ״���������H4SiO4 ��
��2������ڵ�����ҺpH��Ŀ���dz�ȥ�����ӵ����ʣ����Ե���pH���������µ����ʣ����Դ�ѡA����3��pH=4ʱ��������ȫ��������Al3+��ȫ������pH=5.2�����Ե���ҺpH=4ʱ��������ȫ��ȥ������ �� Al3+��
��4����PH=4ʱ����Һ�е����������ӵ�Ũ��Ϊ��1��10-10mol/L����ʱ���������ѳ���������Һ��������ŨΪ��3.2��10-34/(1��10-10)3=3.2��10-4mol/L��Ũ����c��Al3+��=6.4��10-4mol/L����2.25mol/L�����Բ������������������������Ը�ͬѧ�Ĺ۵����
��5����������������Ӧ����ͭ��������ἰ��������Ӧ���ɵ��������ӱ��������������ӣ������������������ӵ�Ũ�Ȼ������䣬�缫��ӦʽΪFe2+- e��=Fe3+��
��6����������л����м���һ��Ũ�ȵ����ᣬʹˮ���е�������Ũ������ƽ�������ƶ���Cu2+����ˮ�����������
��7�����0.1mol CuSO4��Һ������ͭ3.2 g��ת�Ƶ���0.1mol���������������ӷŵ磬����0.025mol������ͬʱ��ʹ��Һ�е�����������0.1mol������Һ���Դ���0.05mol Cu2+��SO42-�����ʵ������䣬����0.1mol�����Դ�ʱ��Һ������Ũ�ȵĴ�С��ϵΪc(H+)>c(SO42-)>c(Cu2+)>c(OH-)��
���㣺���������غ㶨�ɵ�Ӧ�ã��Լ���ѡ�绯ѧԭ����Ӧ�ã���ѧƽ����ƶ�������Ũ�ȵıȽ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡӥ̶����ѧ����ĩ�������߶���ѧ�Ծ��������棩 ���ͣ��ƶ���
(10��)��֪��(X����±��ԭ�ӣ�R��������)

����������Ϣ�������²���� �ϳ�
�ϳ�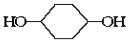 ��(�����Լ��ͷ�Ӧ��������ȥ)
��(�����Լ��ͷ�Ӧ��������ȥ)

��ش��������⣺
��1���ֱ�д��B��D�Ľṹ��ʽ��B____ ��D_ ____ __��
��2����Ӧ�١�����������ȥ��Ӧ����____ _____��(�����ִ���)
��3����������Ǣޡ��߷�Ӧ�����ڷ�Ӧ�ݣ��õ���E���ܵĽṹ��ʽΪ��
_ ��
��4����д��C D��Ӧ�Ļ�ѧ����ʽ(�л���д�ṹ��ʽ����ע����Ӧ����)
D��Ӧ�Ļ�ѧ����ʽ(�л���д�ṹ��ʽ����ע����Ӧ����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����4���������ۻ�ѧ�Ծ��������棩 ���ͣ������
�л�������A�����ϣ��������к�C 72.0����H 6.67�������ຬ�������ִ����������л�������ķ��ӽṹ���������ַ�����
����һ��������������֪A����Է�������Ϊ150��
���������˴Ź����Dz��A�ĺ˴Ź���������5���壬�����֮��Ϊ1��2��2��2��3��
�����������ú�������Dz��A���ӵĺ����������ͼ
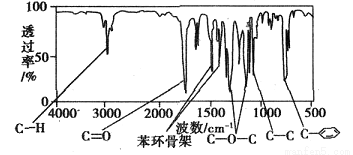
����գ�
��1��A�ķ���ʽΪ____________________��
��2��A�Ľṹ��ʽΪ____________________���������ɣ���
��3��A�ķ�����ͬ���칹���ж��֣����з��������������ٷ��ӽṹ��ֻ��һ�������ţ��ڷ��ӽṹ�к���һ�������۱�����ֻ��һ��ȡ�����������A�ķ�����ͬ���칹�廹��__________�֡�
��4��A��һ��ͬ���칹��E����������������������㾫�ĵ������ϡ��������üױ����Ҵ�Ϊԭ�Ͻ����˹��ϳɡ��ϳ�·�����£�
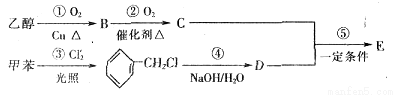
��E�Ľṹ��ʽΪ______________________________��
�ڷ�Ӧ�ڢ۵ķ�Ӧ����Ϊ____________________��____________________��
��д����Ӧ�ٵĻ�ѧ����ʽ________________________________________��
��Ϊ�����E�IJ���Ӧ��ȡ�Ĵ�ʩ��____________________��дһ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ��У�����ڶ����������ۻ�ѧ�Ծ��������棩 ���ͣ������
��13�֣���Щ�������������Ƶ�����ּ���������������̼�������������������ǵ��¼�����������Ҫ���أ��о���Щ��������ۺϴ���������Ҫ���塣
��1����ҵ�Ͽ����ö�����̼�Ͱ����ϳ����أ����ܷ�Ӧ���£�
2NH3(g)+CO2(g)  CO(NH2)2(l)+H2O(l)
CO(NH2)2(l)+H2O(l) 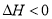 ���÷�Ӧ�� ����ϸ��¶ȡ��ϵ��¶ȡ��������Է����С�
���÷�Ӧ�� ����ϸ��¶ȡ��ϵ��¶ȡ��������Է����С�
��2����֪�ϳ����ط��������У�
��1����2NH3(g)+CO2(g)  NH2COONH4(s)
NH2COONH4(s) 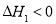
��2����NH2COONH4(s)  CO(NH2)2(l)+ H2O(l)
CO(NH2)2(l)+ H2O(l) 
����ʾ��ͼ��[a��ʾ2NH3(g)+ CO2(g)��b��ʾNH2COONH4(S)��c��ʾCO(NH2)2(l)+ H2O(l)]������ȷ��ʾ���غϳɹ����������仯���ߵ��ǣ�����ţ� ��

��3���ϳ����ع����У���NH3��CO2�����ʵ���֮��Ϊ1:2ʱ��NH3
��ת������ʱ��ı仯��ϵ��ͼ��ʾ��

��A����淴Ӧ����v��(CO2) B����淴Ӧ����
v�� (CO2)(�������������=��)��
�ڴﵽƽ��ʱ��CO2��ת����Ϊ ��
��4������̿�����ڴ���������Ⱦ��NO����ij1L�����ܱ������м��� 0.100molNO ��2.030mol�������̿�������ʣ�����������E������F�����¶ȷֱ���T1���T2��ʱ�����ƽ��ʱ�����ʵ����ʵ������±���
n/mol T/�� | ����̿ | NO | E | F |
T1 | 2.000 | 0.040 | 0.030 | 0.030 |
T2 | 2.005 | 0.050 | 0.025 | 0.025 |
�������ϱ����ݣ�д��NO�����̿��Ӧ�Ļ�ѧ����ʽ ��
��������Ӧ��T1��ʱ��ƽ�ⳣ��ΪK1����T2��ʱ��ƽ�ⳣ��ΪK2������K1= �����������Ϣ�жϣ�T1��T2�Ĺ�ϵ�� ��
A. T1>T2B. T1<T2C.���Ƚ�
�����ܱ�����Ϊ�ݻ��ɱ䣬���ݻ�ѧ��Ӧԭ������������ѹǿ�Ը÷�Ӧ��Ӱ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ��У�����ڶ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��PX�����Զ��ױ�, ��һ�ֿ�ȼ���Ͷ�����������Ը����Ҵ�����������������γɱ�ը�Ի�����ը����1.1%��7.0%���������������һ����;������л�����ԭ�����й��ڡ�PX������������ȷ���� �� ��
A����PX���Ļ�ѧʽΪC8H10��1H-NMR��2�����շ�
B����PX����ʹ���Ը��������Һ��ɫ�����ڱ���ͬϵ��
C����PX�����������3��ͬ���칹��
D����PX�� ������ˮ���ܶȱ�ˮС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡЭ��������ڶ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȼ�ϵ��Ϊ��Դ���е���ʵ��װ������ͼ��ʾ������˵����ȷ����( )
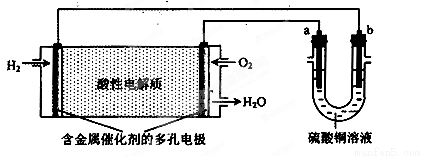
A�� a������b����
B����a��������b����ͭ��b�����ܽ⣬a������ͭ����
C����a��b������ʯī������ͬ�����£�������a���������������������ĵ�O2������
D������⾫����ͭʱ��b���Ǵ�ͭ��a���Ǵ�ͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ������У����5���������ۻ�ѧ�Ծ��������棩 ���ͣ������
����ѧѡ��-��ѧ�뼼����(15��)
��ʯ�����ȼҵ�е�һ�ַ���������������±���ʾ��

�õ�ʯ����������ˮCaCl2��ij��������������¹������̣�
��֪�Ȼ��ƾ���Ļ�ѧʽ�ǣ�CaCl2��6H2O��H2S��һ���������壬�Ҿ��л�ԭ�ԡ�
�ŷ�Ӧ���м������Ӧѡ��___________________��
����ɫ����Ӧ���������X��_______________���豸A��������______________���豸B������Ϊ________________���豸C��������____________________��
��Ϊ�����㻷��Ҫ���轫����H2Sͨ�����ճأ��������������ʺ���Ϊ���ռ�����____________ _����Ӧ�Ļ�ѧ����ʽΪ_________________��
A��ˮ B��Ũ���� C��ʯ���� D������
�Ƚ��豸B�в�����ĸҺ�������뷴Ӧ����Ŀ����______________________��
���ȼҵ���ӷ���ʽ_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�˴��и���ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���ݱ�����Ϣ�жϣ�����ѡ����ȷ���ǣ� ��

A���ڢ��鷴Ӧ���������ΪH2O
B���ڢ��鷴Ӧ��Cl2��FeBr2�����ʵ���֮��С�ڻ����1��2
C���ڢ��鷴Ӧ������1mol Cl2��ת�Ƶ���5mol
D����������ǿ����˳��ΪMnO4 >Cl2> Fe3+> Br2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�ϲ��и�һ�����ֿƲ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��̽�����Ʊ�����ˮ�ɷֵ�ʵ���У����и���ʵ������ó��Ľ��۲���ȷ����
A����ˮ����ɫ��dz��ɫ��˵����ˮ�к���Cl2
B������ˮ�еμ������ữ��AgNO3��Һ��������ɫ������˵����ˮ�к���Cl��
C������ˮ�м���NaHCO3��ĩ�������ݲ�����˵����ˮ�к���H��
D����FeCl2��Һ�еμ���ˮ����Һ��ɫ����ػ�ɫ��˵����ˮ�к���HClO
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com