
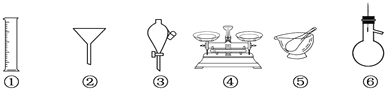
| A. | ①③⑥ | B. | ②④⑥ | C. | ②③⑥ | D. | ②③⑤ |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 结合Na、Al、Fe的有关性质,回答下列问题.
结合Na、Al、Fe的有关性质,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu→CuSO4 | B. | C→CO2 | C. | CuO→CuSO4 | D. | Fe2O3→Fe2(SO4)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置①中K键闭合时,片刻后可观察到滤纸a点变红色 | |
| B. | 装置①中K键闭合时,片刻后CuSO4溶液中c(Cl-)增大 | |
| C. | 装置②中铁腐蚀的速度由大到小的顺序是:只闭合K1>只闭合K3>只闭合K2>都断开 | |
| D. | 装置③中当铁制品上析出1.6 g铜时,电源负极输出的电子数为0.025 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 46 | B. | 34 | C. | 30 | D. | 60 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:W>X>Y>Z | B. | 原子半径:W>X>Y>Z | ||
| C. | W的最高价氢氧化物的碱性比X弱 | D. | Y的最简单氢化物的稳定性比Z的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制饱和氯水中:Na+、Al3+、SO32-、SO42- | |
| B. | 加入铝粉能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42- | |
| C. | 常温下,在碱性的溶液中:K+、AlO2-、CO32-、Na+ | |
| D. | 在碱性的溶液中:K+、NH4+、AlO2-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在7.8gNa2O2晶体中阳离子与阴离子总数为0.3NA | |
| B. | 在KIO3+6HI=KI+3I2+3H2O反应中,每生成3mol I2,则转移6NA个电子 | |
| C. | 1mol Na2O2与H2O完全反应,转移的电子总数为NA | |
| D. | 在1L0.1mol/L的碳酸钠溶液中,阴离子总数大于0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com