
下列实验设计方法正确的是( )
A.向卤代烃加硝酸酸化的硝酸银来检验其中的卤族素元素
B.实验用NH4Cl固体受热分解来制备NH3
C.用盐酸和澄清石灰水来检验某物质是否含有CO32-
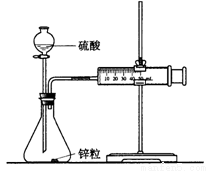
D.可用下图所示的装置和药品来研究反应物浓度对反应速率的影响
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源:2015届福建省高二上学期半期联考化学试卷(解析版) 题型:选择题
对于反应A2(g)+ 3B2(g) 2C(g),以下表示其化学反应速率最快的是
2C(g),以下表示其化学反应速率最快的是
A.v(A2) =0.4mol/(L?s) B.v(B2) =0.8mol/(L?s)
C.v(C) =0.6mol/(L?s) D.v(B2) =4.2mol/(L?min)
查看答案和解析>>
科目:高中化学 来源:2015届福建省高一上学期半期联考化学试卷(解析版) 题型:选择题
下列各组物质的溶液混合后,再加足量的稀硝酸,仍有沉淀存在的是
A.K2CO3、BaCl2 B.NaOH、CuSO4
C.AgNO3、NaCl D.Na2CO3、CaCl2
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三9月月考化学试卷(解析版) 题型:填空题
(16分)氨既是实验室中常用试剂,也是工业上重要原料。
(1)某学习小组欲制备少量的氨水。供选用的试剂有:
①NH4Cl ②(NH4)2CO3 。提供的装置如下,请回答下列问题:
①装置A试管内发生反应的化学方程式为 ;
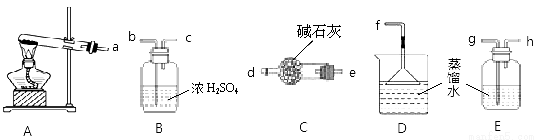
②从提供的仪器中选择并组装一套本实验的合理、简洁装置,按气流方向连接顺序为(用图中标注的导管口符号表示)a→ ;
(2)氨在氧气中燃烧,生成水和一种单质。
已知: N2(g)+3H2(g) 2NH3(g) △H= -92.4kJ·mol-1
2NH3(g) △H= -92.4kJ·mol-1
2H2(g)+ O2(g)= 2H2O(l) △H= -572kJ·mol-1
写出氨在氧气中燃烧生成液态水和气态单质的热化学方程式: ;
(3)已知在一定条件下,将1molN2和3molH2混合于一个10L的密闭容器中发生的
反应为N2+3H2 2NH3,5min后达到平衡,平衡时氨的体积分数为25%。
2NH3,5min后达到平衡,平衡时氨的体积分数为25%。
①该反应的平衡常数表达式K = ;
②从反应开始到平衡时,N2的反应速率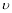 (N2)= _________________;
(N2)= _________________;
(4)工业上以氨气、空气为主要原料制取硝酸。在容积恒定的密闭容器中进行反应2NO(g)+O2(g) 2NO2(g) △H>0。该反应的反应速率(
2NO2(g) △H>0。该反应的反应速率(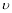 )随时间(
)随时间( )变化的关系如图所示。若
)变化的关系如图所示。若 时刻只改变一个条件,下列说法正确的是(填选项序号) 。
时刻只改变一个条件,下列说法正确的是(填选项序号) 。

A.在 时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
B.在 时,采取的措施可以是升高温度
时,采取的措施可以是升高温度
C.在 时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
D.在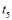 时,容器内
时,容器内 的体积分数是整个过程中的最大值
的体积分数是整个过程中的最大值
(5)为检验氨气与酸反应得到的某种常见氮肥的成分,某同学进行了以下实验:
①加热氮肥样品产生气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊。②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化。由此可知该氮肥的主要成分可能是_____________(填选项序号);
A.NH4Cl B.(NH4)2CO3 C.NH4HCO3 D.NH4NO3
(6)硝酸厂常用Na2CO3溶液吸收处理尾气NO2生成CO2。若9.2g NO2和Na2CO3溶液完全反应时转移电子0.1mol,则反应的离子方程式是:
。
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三9月月考化学试卷(解析版) 题型:选择题
有一块铁的“氧化物”样品,用140mL 5.0mol·L-1 盐酸恰好将之完全溶解,所得溶液还能吸收0.025mol Cl2,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
A.Fe2O3 B.Fe3O4 C.Fe4O5 D.Fe5O7
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三9月月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.0.1 mol·L-1Na2S溶液中含有的Na+离子数为0.2NA
B.50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA
C.标准状况下,22.4 L以任意比例混合的氢气和氯气混合气中含有的原子总数为2NA
D.0.10 mol Fe粉与足量水蒸气反应生成的H2分子数为0.10NA
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三10月月考理综化学试卷(解析版) 题型:填空题
【化学——选修3 物质结构基础】(15分)
氧元素与多种元素具有亲和力,所形成化合物的种类仅次于碳元素。
(1)氮、氧、氟元素的第一电离能从大到小的顺序为 ,氧元素与氟元素能形成OF2分子,该分子的空间构型为 。
(2)根据等电子原理,判断NO2+离子中,氮原子轨道的杂化类型为 ,1mol NO2+所含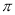 键的数目为 。
键的数目为 。
(3)氧元素与过渡元素可以形成多种价态的金属氧化物。如铬可生成Cr2O3、CrO3等,试写出Cr3+核外电子排式 。
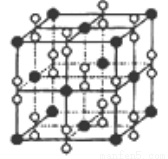
(4)钙在氧气中燃烧时得到一种钙的氧化物晶体,其结构如图所示:由 此可判 断该钙的氧化物的化学式为 。
已知晶胞边长为540pm,则该氧化物的密度是 g·cm-3
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三上学期第二次检测考试化学试卷(解析版) 题型:选择题
取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生8960 mL的NO2气体和672 mLN2O4的气体(都已折算到标准状态),在反应后的溶液中加足量的氢氧化钠溶液,生成沉淀质量为17.02g。则x等于
A.8.64g B.9.20g C.9.00g D.9.44g
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三第一次诊断考试化学试卷(解析版) 题型:填空题
(10分)在Na+浓度为0.5mol/L的某澄清溶液中,还可能含有下表中的若干种离子:
阳离子 | K+、Ag+、Mg2+、Ba2+ |
阴离子 | NO3-、CO32-、SiO32-、SO42- |
取该溶液100mL进行如下实验(气体体积在标准状况下测定):
序号 | 实验内容 | 实验结果 |
Ⅰ | 向该溶液中加入足量稀HCl | 产生白色沉淀并放出0.56L气体 |
Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
Ⅲ | 在Ⅱ的滤液中滴加BaC12溶液 | 无明显现象 |
试回答下列问题:
(1)实验I能确定一定不存在的阳离子是 。
(2)实验I中生成沉淀的离子方程式为 。
(3)通过实验I、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)
阴离子 | NO3- | CO32- | SiO32- | SO42- |
c/mol·L-1 |
|
|
|
|
(4)判断K+是否存在,若存在求其最小浓度,若不存在说明理由 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com