
下列曲线中,可以描述乙酸(甲,Ka=1.8×10-5)和一氯乙酸(乙,Ka=1.4×10-3)在水中的电离度与浓度关系的是( )
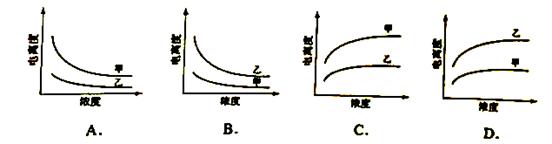
【答案】B
【解析】A、根据题给电离常数分析醋酸和一氯醋酸均为弱电解质且在相同温度、相同浓度时,醋酸的电离度小于一氯醋酸,即甲的电离度小于乙;弱电解质的浓度越大,电离度越小,与图像不符,错误;B、根据题给电离常数分析醋酸和一氯醋酸均为弱电解质 且在相同温度、相同浓度时,醋酸的电离度小于一氯醋酸,即甲的电离度小于乙;弱电解质的浓度越大,电离度越小,与图像相符,正确;C、根据题给电离常数分析醋酸和一氯醋酸均为弱电解质且在相同温度、相同浓度时,醋酸的电离度小于一氯醋酸,即甲的电离度小于乙;弱电解质的浓度越大,电离度越小,与图像不符,错误;D、根据题给电离常数分析醋酸和一氯醋酸均为弱电解质且在相同温度、相同浓度时,醋酸的电离度小于一氯醋酸,即甲的电离度小于乙;弱电解质的浓度越大,电离度越小,与图像不符,错误。
且在相同温度、相同浓度时,醋酸的电离度小于一氯醋酸,即甲的电离度小于乙;弱电解质的浓度越大,电离度越小,与图像相符,正确;C、根据题给电离常数分析醋酸和一氯醋酸均为弱电解质且在相同温度、相同浓度时,醋酸的电离度小于一氯醋酸,即甲的电离度小于乙;弱电解质的浓度越大,电离度越小,与图像不符,错误;D、根据题给电离常数分析醋酸和一氯醋酸均为弱电解质且在相同温度、相同浓度时,醋酸的电离度小于一氯醋酸,即甲的电离度小于乙;弱电解质的浓度越大,电离度越小,与图像不符,错误。
【考点定位】考查弱电解质的电 离。
离。
【名师点睛】本题将弱电解质的电离常数及影响电离平衡的外界因素与图像结合在一起考查了学生对弱电解质电离常数、电离度的意义、浓度对弱电解质的电离的影响等基础知识掌握的熟练程度,又结合图像考查了 学生的观察能力和思维能力。难度中等。
学生的观察能力和思维能力。难度中等。


科目:高中化学 来源: 题型:
生活中常常碰到涉及化学知识的某些问题,下列叙述正确的是( )
①人的皮肤在强紫外线的照射下将会失去生理活性
②用甲醛溶液浸泡海产品保鲜
③变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应
④棉花和木材的主要成分都是纤维素,禽类羽毛和蜘蛛丝的主要成分都是蛋白质
⑤蜂蚁叮咬人的皮肤时将分泌物甲酸注入人体,此时可在患处涂抹小苏打或稀氨水
⑥利用油脂在碱性条件下水解,可以生产甘油和肥皂
⑦室内装饰材料中缓慢释放出的甲醛、苯等有机物会污染空气
A.①④⑤⑥⑦ B.②③④⑥
C.①②④⑤⑦ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是( )
A.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO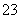 和OH-
和OH-
B.NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-)
C.10 mL 0.10 mol·L-1 CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
I.二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的杀菌消毒剂,被称为“第4代消毒剂”。
(1)工业上采用氯酸钠制备ClO2:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①浓盐酸在反应中显示出来的性质是 (填字母序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②当生成0.4molClO2时,转移电子 mol。
③若采用双氧水还原氯酸钠制备ClO2,更适合用于饮用水的消毒,其主要原因是 。
(2)ClO2在杀菌消毒的同时,可将剧毒氰化物氧化成无毒气体而除去,写出用ClO2
氧化除去CN-的离子方程式 。
II.下图甲是用H2还原 CO2制备甲醇的原电池工作原理示意图;图乙是用图甲作电源实现CO2制备碳氢化物的工作原理示意图(用KHSO4溶液作电解液)。
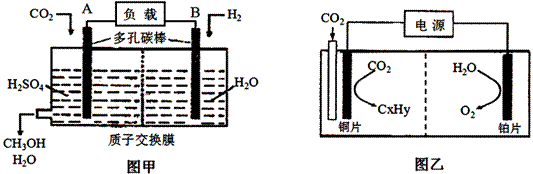
(1)图甲中A的电极名称是 。
(2)若乙中碳氢化物为C2H4, 则铜电极的电极反应为 。
(3)若通入的CO2全部参加反应,甲乙中共消耗0.6molCO2 时,图甲中通过质子交换膜的H+ 的物质的量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下向10mL0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA溶液pH的变化曲线如图所示。下列说法正确的是( )
A.a点所示溶液中c(Na+)>c(A—)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)= c(A—)+ c(HA)
D.b点所示溶液中c(A—)> c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
氨是合成硝酸、铵和氮肥的基本原料,回答下列问题:
(1)氨的水溶液显弱碱性,其原因为 (用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的PH (填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度 (填“增大”或“减小”)。
 (2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 ,平衡常数表达式为 ;若有1mol硝酸铵完全分解,转移的电子数为 mol。
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 ,平衡常数表达式为 ;若有1mol硝酸铵完全分解,转移的电子数为 mol。
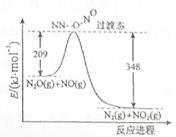
(3)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1molN2, 其△H= kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g) 
 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
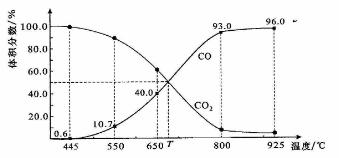
已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是( )
A.550℃时,若充入惰性气体,ʋ正,ʋ逆 均减小,平衡不移动
B.650℃时,反应达平衡后CO2的转化率为25.0%
C.T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数KP=24.0P总
查看答案和解析>>
科目:高中化学 来源: 题型:
向各盛有1L水的甲、乙、丙、丁四个烧杯内分别加入等物质的量的Na、Na2O、Na2O2和NaOH,固体完全溶解后,各烧杯中溶质的质量分数大小顺序是()
| A. | 甲<乙<丙<丁 | B. | 丁<甲<乙=丙 | C. | 甲=丁<乙=丙 | D. | 丁<甲<丙<乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
今有如下三个热化学方程式:
H2(g)+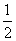 O2(g)===H2O(g) ΔH=a kJ·mol-1
O2(g)===H2O(g) ΔH=a kJ·mol-1
H2(g)+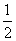 O2(g)===H2O(l) ΔH=b kJ·mol-1
O2(g)===H2O(l) ΔH=b kJ·mol-1
2H2(g)+O2(g)===2H2O(l) ΔH=c kJ·mol-1
下列关于他们的表述正确的是( )
A.它们都是吸热反应 B.a、b和c均为正值
C.a=b D.2b=c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com