
 ��ˮAlCl3��һ����Ҫ�Ļ���ԭ�ϣ�ij����̽��С�鳢����ȡ��ˮAlCl3���������ϻ��������Ϣ����ˮAlCl3��178�����������׳��⣬��ˮ����������ɫ������
��ˮAlCl3��һ����Ҫ�Ļ���ԭ�ϣ�ij����̽��С�鳢����ȡ��ˮAlCl3���������ϻ��������Ϣ����ˮAlCl3��178�����������׳��⣬��ˮ����������ɫ������| ��һ��ʵ�� | �ڶ���ʵ�� | ������ʵ�� | |
| D������� | 2.0g | 2.0g | 2.0g |
| ��������� | 334.5mL | 336.0mL | 337.5mL |
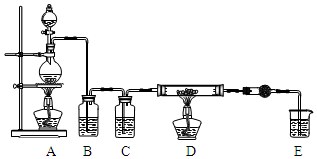
���� ��������飬�Ʊ��Ȼ������Ȼ����Ĵ��ȷ�����̽��ʵ�����������ķ�Ӧԭ���������Ȼ����Ʊ������ö������̺�Ũ�����ϼ����Ƶ����������۹����Ʊ��Ȼ�����ʵ�������Ҫ��ע�����ľ���������������������ֹ�����������������ﻷ�������Ȼ���ˮ�⣩��������β���������ٶԻ�������Ⱦ���Ȼ�����Ʒ�п��ܻ�������������������������Һ��Ӧ���ɵ������ⶨ���ĺ������ټ�����Ȼ����Ĵ��ȣ�̽��ʵ�����Ʊ�������ԭ���ɴ����������������1��������Ũ�ȶ�ʵ���Ӱ�죨2��H+��ʵ���Ӱ�죻
��1��ʵ���������ö���������Ũ�����ϼ����������ģ��ɾݴ�д����Ӧ��ѧ����ʽ��
��2��ʵ��ǰװ�����������������ʱ���������������������ɵ�������ȥ�������Ƶõ��Ȼ����л���������������ݴ�˼·ȷ������˳��
��3����ˮAlCl3��ˮ������������ˮ�ⷴӦ��
��4����������ʵ�����ɵ�������ƽ��ֵ���ٸ������ɵ���������μӷ�Ӧ���������ɼ�����Ȼ���������������
��5���Ȼ����ĺ���ƫ�ͣ������ֲ��μӷ�Ӧ�����⣬�������в�����������������
��� �⣺��1��ʵ�����ö���������Ũ���ᷴӦ�������ķ�Ӧ����ʽΪMnO2+4HCl$\frac{\underline{\;����\;}}{\;}$MnCl2+Cl2��+2H2O���ʴ�Ϊ��MnO2+4HCl$\frac{\underline{\;����\;}}{\;}$MnCl2+Cl2��+2H2O��
��2��ʵ�鿪ʼǰ���ȼ��װ�������ԣ�Ȼ��װ��ҩƷ��������������Ũ�����ټ���A�оƾ��ƣ���Ӳ�ʲ������г�������ɫ������ټ���Dװ�ã���ȷ����˳��Ϊbca���ʴ�Ϊ��bca��
��3����ˮ�Ȼ�����ˮ������Al3+��ˮ�������������·�Ӧ���ٽ��У���Ӧ����ʽΪAlCl3+3H2O��g��=Al��OH��3+3HCl���ʴ�Ϊ��AlCl3+3H2O��g��=Al��OH��3+3HCl��
��4������ʵ���ռ���������ƽ��ֵΪ��334.5mL+336.0mL+337.5mL����3=336.0mL�����������ʵ���Ϊ$\frac{336��1{0}^{-3}L}{22.4L/mol}$=0.015mol������2Al��3H2����֪�������ʵ���Ϊ$\frac{0.015mol��2}{3}$=0.01mol������Ϊ0.01mol��27g/mol=0.27g���Ȼ�������������Ϊ$\frac{2.0g-0.27g}{2.0g}$=86.5%���ʴ𰸣�86.5%��
��5�����������㣬������δ��Ӧ�����Ȼ������ɵ����Ȼ�������ƫ�ͣ��������������ֽӴ�����������δ�������������������������Ȼ�������ƫ�ͣ��������Ȼ���������Ҳ�ܵ����Ȼ�������ƫ�ͣ��ʴ�Ϊ���٢ڢۣ�
���� �����ۺϳ̶Ƚϸߣ��������������Ȼ������Ʊ���̽�����Ȼ��������ⶨ�������Ʊ�ԭ�����漰���ʵ������㡢ʵ�������ѡ��ȣ�֪ʶ��㣬���Ѷ��еȣ���ѧ������Ҫ��ϸߣ���ѧ���Ľ������������һ��������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
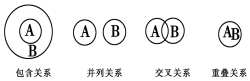
| A�� | ���������������ڰ�����ϵ | |
| B�� | ������ԭ��Ӧ�뻯�Ϸ�Ӧ���ڰ�����ϵ | |
| C�� | ��Һ���ɢϵ���ڲ��й�ϵ | |
| D�� | ��������������������ڽ����ϵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| �¶ȡ� | 700 | 800 | 880 | 1000 | 1200 |
| ƽ�ⳣ�� | 1.0 | 10.0 | 15.0 | 16.1 | 17.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
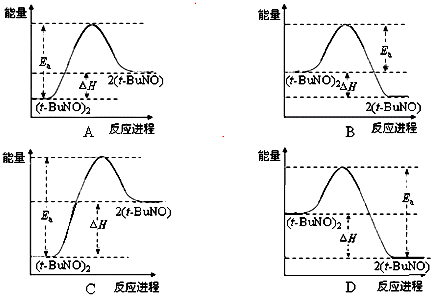
 �������ѧ֪ʶ�ش��������⣺
�������ѧ֪ʶ�ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
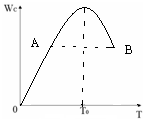 ���ڷ�Ӧ2A��g��+B��g��?2C��g���ڷ�Ӧ������C��������WC���¶ȱ仯��ͼ��ʾ����ȷ����
���ڷ�Ӧ2A��g��+B��g��?2C��g���ڷ�Ӧ������C��������WC���¶ȱ仯��ͼ��ʾ����ȷ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
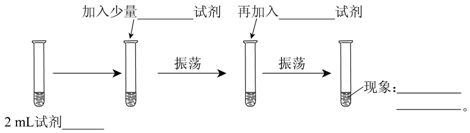
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl3 | B�� | Fe2O3 | C�� | Fe��OH��3 | D�� | Fe3O4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com