
【题目】36.5gHCl溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为w,物质的量浓度为cmol/L,NA表示阿伏加德罗常数的值,则下列叙述中正确的是( )
A. 所得溶液的物质的量浓度:c=1mol/LB. 所得溶液中含有NA个HCl分子
C. 36.5gHCl气体占有的体积为22.4LD. 所得溶液的质量分数w=![]()
科目:高中化学 来源: 题型:
【题目】有关物质的量的计算是中学化学的重要内容,完成以下填空:
(1)0.5 L 1 mol/L CaCl2溶液中Ca2+的物质的量为_______,Cl的物质的量浓度为_______。
(2)标准状况下,33.6 L的HCl所具有的物质的量为______,将其溶解于水配成3 L的溶液,所得盐酸的物质的量浓度为______。
(3)8 g NaOH溶于______g水中,才能使每10个水分子中溶有一个钠离子。
(4)49 g H2SO4中含______mol原子,含______个质子。
(5)标准状况下,2.4 g某气体的体积为672 mL,则此气体的相对分子质量为_______。
(6)在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,若其中CO和N2的物质的量之比为1∶1,则混合气体中氧元素的质量分数为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求书写方程式
(1)过氧化钠与CO2反应的化学方程式:___;
(2)将少量硫酸铝溶液滴入足量氨水中的离子方程式:___;
(3)铁与水蒸气反应的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某透明的酸性溶液中,因发生氧化还原反应而不能大量共存的是( )
A. NO3-、Cl-、Fe2+、Na+B. Ag+、NO3-、Cl-、K+
C. K+、Ba2+、OH-、SO42-D. Cu2+、NH4+、Br-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列环境问题与所对应的物质不相关的是( )
A. 温室效应——二氧化碳B. 光化学烟雾——二氧化氮
C. 酸 雨——二氧化硫D. 臭氧层破坏——一氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甘氨酸锌是一种新型食品营养强化剂,可由ZnO与甘氨酸 制备。
制备。
(1)Zn2+基态核外电子排布式为__________________。
(2)甘氨酸分子中碳原子轨道的杂化类型是________________,1mol 甘氨酸分子中含有σ键的数目为________________。
(3)以氧化锌矿物为原料,提取锌的有关反应为:ZnO+2NH3+2NH4+= [Zn(NH3)4]2++H2O。与NH4+互为等电子体的阴离子为_____,[Zn(NH3)4]2+的结构可用示意图表示为______________。
(4) 闪锌矿的主要成分是一种锌的硫化物,其晶胞结构如图所示,其化学式为___________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将饱和氯化铁溶液滴入沸水时,液体变为________色,得到的是________,反应的化学方程式为__________________________________________。用此分散系进行实验:
(1)将其装入U形管内,用石墨作电极,接通直流电源,通电一段时间后发现阴极附近颜色________,这表明________,这种现象称为________。
(2)向其中加入饱和的硫酸铵溶液,发生的现象是____________,原因是____________________。
(3)向其中逐滴加入过量稀硫酸,现象是_________________,原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学键的叙述,正确的是
A.离子化合物中一定含有离子键
B.单质分子中均存在化学键
C.由不同种非金属元素的原子形成的共价化合物一定只含极性键
D.含有共价键的化合物一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是组成人体细胞的主要元素及其比例,下列相关叙述中,错误的是( )
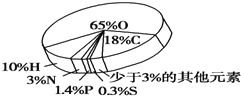
A.图中所示为细胞鲜重中元素的比重
B.因为O元素含量最多,所以O元素是构成有机物的根本元素
C.细胞失去大部分水分后,C元素比重最大
D.图中含有的元素在非生物界也可以找到
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com