
【题目】二水合重重铬酸钠(Na2Cr2O7.2H2O),[已知M(Na2Cr2O7.2H2O)=298g/mol]俗称红矾钠,在工业方面有广泛用途。我国目前主要是以铬铁矿(主要成份为FeO.Cr2O3,还含有A1203、MgO、Si02等杂质)为主要原料生产,其主要工艺流程如图:
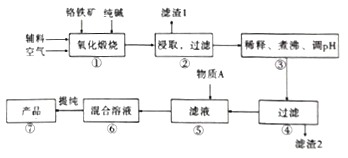
已知信息:
Ⅰ.“①”中涉及的主要反应是:4FeO·Cr2O3+8Na2CO3+7O2=8Na2CrO4+2Fe2O3+8CO2
Ⅱ.部分阳离子以氢氧化物形式完全沉淀时溶液的PH如下:
沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
完全沉淀时溶液PH | 4.7 | 3.7 | 11.2 | 5.6 |
(1).杂质A12O3、SiO2与纯碱反应转变为可溶性盐,写出A12O3纯碱反应的化学方程式为:______________,滤渣1的主要成分为__________________。
(2).“③”中通过调节PH除去杂质,调节PH至___________。
(3).“⑤”中向滤液中加入物质A,得到Na2Cr2O3和Na2SO4的混合溶液,物质A为__________,简述原因:______________________________。(用离子方程式及文字加以说明)
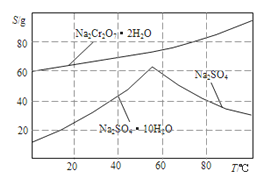
(4).如图是Na2Cr2O3.2H2O和Na2SO4的溶解度曲线。提纯的实验操作:将Na2Cr2O3和Na2SO4的混合溶液______________________,得到Na2SO4固体和较纯净的Na2Cr2O3溶液。
(5).实验室测定所得产品中红矾钠的纯度,称取产品3.2g,配成250mol溶液,取出25.00mL于锥形瓶中,加入10mL2mol/LH2SO4和足量碘化钾,放于暗处5min,写出离子方程式:________________。然后加水100mL,加入3mL淀粉指示剂,用0.1000mol/LNa2S2O3标准溶液滴定I2+2S2O32-=2I-+S4O62-若达到滴定终点时,共用去Na2S2O3标准溶液60mL,所得产品的纯度是_________(结果保留小数点后1位)。
【答案】(1).Al2O3+Na2CO3![]() 2NaAlO2+CO2↑(2分)Fe2O3、MgO(2分)(2).4.7(2分)
2NaAlO2+CO2↑(2分)Fe2O3、MgO(2分)(2).4.7(2分)
(3).H2SO4(1分)2CrO42-![]() Cr2O72-+H2O,加入硫酸,平衡向右移动(1分)
Cr2O72-+H2O,加入硫酸,平衡向右移动(1分)
(4).蒸发浓缩、趁热过滤(5).14H++Cr2O72-=2Cr3+3I2+7H2O(2分)93.1%
【解析】
试题分析:(1)A12O3与纯碱反应的化学方程式为Al2O3+Na2CO3![]() 2NaAlO2+CO2↑;氧化亚铁被氧化为氧化铁,氧化镁没有参与反应,因此滤渣1的主要成分为Fe2O3、MgO。
2NaAlO2+CO2↑;氧化亚铁被氧化为氧化铁,氧化镁没有参与反应,因此滤渣1的主要成分为Fe2O3、MgO。
(2)“③”中通过调节pH除去杂质,根据氢氧化铝的沉淀pH范围可知调节pH至4.7。
(3)“⑤”中向滤液中加入物质A,得到Na2Cr2O3和Na2SO4的混合溶液,物质A为H2SO4,这是由于溶液中存在平衡:2CrO42-![]() Cr2O72-+H2O,加入硫酸,平衡向右移动;
Cr2O72-+H2O,加入硫酸,平衡向右移动;
(4).根据Na2Cr2O3.2H2O和Na2SO4的溶解度曲线可知硫酸钠的溶解度随温度的升高而升高,但超过60℃后反而降低,因此提纯的实验操作为:将Na2Cr2O3和Na2SO4的混合溶液蒸发浓缩、趁热过滤,得到Na2SO4固体和较纯净的Na2Cr2O3溶液。
(5).重铬酸根离子氧化碘离子的方程式为实验室测定所得产品中红矾钠的纯度,称取产品3.2g,配成250mol溶液,取出25.00mL于锥形瓶中,加入10mL2mol/LH2SO4和足量碘化钾,放于暗处5min,反应的离子方程式为14H++Cr2O72-=2Cr3+3I2+7H2O。根据方程式可知Cr2O72-~3I2~6S2O32-,所以所得产品的纯度是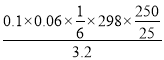 ×100%=93.1%。
×100%=93.1%。


科目:高中化学 来源: 题型:
【题目】已知吸热反应2CO(g) = 2C(s)+O2(g) ,设ΔH 和ΔS不随温度而变,下列说法中正确的是
A. 低温下能自发进行 B. 高温下能自发进行
C. 任何温度下都能自发进行 D. 任何温度下都不能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙为常见单质。A、B、C、D、E、F、G、H均为中学化学中常见的化合物,其中B、G的焰色反应均为黄色,C能使品红溶液褪色。在一定条件下,各物质相互转化关系如图所示。
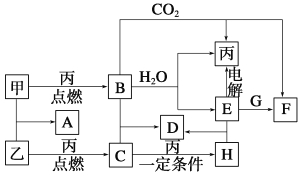
请回答下列问题:
(1)用化学式表示:丙为__________,H为__________。
(2)A的电子式为________________________________。
(3)电解E的水溶液时,E起到的作用是_______________________
(4)写出B+C―→D的化学方程式______________________________
写出E+G―→F的离子方程式___________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
(已知N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g) ![]() kJ·mol
kJ·mol![]() )
)
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
NH3的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
体系压强(pa) | p1 | p2 | p3 |
反应物转化率 | α1 | α2 | α3 |
请写出下列物理量的关系:
(1)浓度c1与c2__________________2c2与c3 ________________
(2)能量a与b __________________2b与c___________________
(3)压强p1与p2_________________2p2与p3 __________________
(4)转化率α1与α2_________________α2与α3___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体硝酸盐加热易分解且产物较复杂,某学习小组以Fe(NO3)2为研究对象,通过实验探究其热分解的产物,查阅资料,根据硝酸盐受热分解的规律,提出如下4种猜想:
甲:Fe2O3、NO2乙:Fe2O3、NO2、O2丙:Fe3O4、NO2、O2丁:FeO、NO2、N2
(1).实验前,小组成员经讨论认定猜想丁不成立,理由是__________________.
针对上述猜想,设计如图所示的实验装置(图中加热、夹持仪器等均省略):
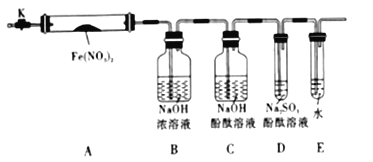
(2).实验过程
①仪器连接后,放人固体试剂之前,应______________
②称取Fe(NO3)2固体3.6g置于A中,加热前先打开K,___________,后再关闭K,用酒精灯加热
③观察到A中有红棕色气体出现,C、D中未见明显变化.
④待样品完全分解,A装置冷却至室温、称量,测得剩余固体的质量为1.6g
⑤取少量剩余固体于试管中,加人适量水,未见明显现象.
(3).实验结果分析讨论:
①根据实验现象和剩余固体的质量经分析,可初步确认分解产物中有____________。
②根据D中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中溶液颜色会退去;另一个同学认定分解产物中有O2存在,未检侧到的原因是_________________。
③为了验证是否有O2,某同学另称Fe(NO3)2固体3.6g,充分加热,收集气体,假设产生的气体全部收集,将集满气体的试管倒放在水槽中,观察到的现象是红棕色消失,液面上升,进入试管中的溶液大于2/3,通入一定量的O2后,气体全部被吸收,请写出Fe(NO3)2受热分解的化学方程式______________,通入O2的物质的量为_____________。
④小组讨论后达成的共识是上述实验设计仍不完善,需改进装置进一步研究。写一点不足之处:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对已达化学平衡的下列反应2X(g)+Y(g)![]() 2Z(g),减小压强时,对反应产生的影响是( )
2Z(g),减小压强时,对反应产生的影响是( )
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒电池以惰性材料作电极,在电解质溶液中发生的电池总反应为:VO2+(蓝色)+H2O+V3+(紫色)![]() VO2+(黄色)+V2+(绿色)+2H+ 下列说法错误的( )
VO2+(黄色)+V2+(绿色)+2H+ 下列说法错误的( )
A. 充电时,反应每生成2molH+时电子转移的物质的量为2mol
B. 放电过程中,正极附近溶液的酸性减弱
C. 放电时,正极反应为VO2++2H++e-=VO2++H2O
D. 充电时,阳极附近溶液由蓝色逐渐变为黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于组成细胞的化学元素和化合物的说法中,错误的是
A. 胰岛素和性激素的化学本质分别是蛋白质和固醇
B. 休眠的种子细胞中结合水与自由水比值下降,有利于种子的储藏
C. 蛋白质的基本组成单位是氨基酸,组成蛋白质的氨基酸种类约有20种
D. 动物与植物细胞所含的化学元素的种类大体相同,但含量有差异
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com