
�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��1����ҵ��һ������������ַ�Ӧ�ϳɼ״���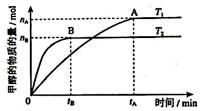
��ӦI�� CO(g)+2H2(g) CH3OH(g) ��H1
CH3OH(g) ��H1
��ӦII�� CO2(g)+3H2(g) CH3OH(g)+ H2O(g) ��H2
CH3OH(g)+ H2O(g) ��H2
��������Ӧ���ϡ�ԭ�Ӿ��á�ԭ����� (�I����)��
���������������������£������¶ȶԷ�ӦII��Ӱ�죬ʵ������ͼ��ʾ
��ͼ�������ж� ��H2 0 (���������=������)��
��ij�¶��£���2 mol CO2��6 mol H2����2L���ܱ������У�������ӦII���ﵽƽ����c(CO2)= 0��2 mol/L�� ���ʱ�����е�ѹǿΪԭ���� ��
��2����֪�ڳ��³�ѹ�£�
�� 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ��H =-1275��6 kJ/mol
�� 2CO (g)+ O2(g) = 2CO2(g) ��H =-566��0 kJ/mol
�� H2O(g) = H2O(l) ��H =-44��0 kJ/mol
�����1 mol�״�����ȫȼ������1 molһ����̼��Һ̬ˮ�ų�������Ϊ ��
��3��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ���������ͼ��ʾ�ĵ��װ�ã�
�ٸõ�ظ����ĵ缫��ӦΪ
�ڴ˵�����ļ״�1��6��ʱ����Ӧ�е���ת����ĿΪ
�����Դ�ȼ�ϵ��ΪǦ���س�磬��Ӧ��ͼ���Ҳ�缫�������ص� (��������)
��1�� �� I �� < �� 0��6 ��2��442��8 KJ ��3��CH3OH+8OH- -6e- = CO32- +6H2O0��3NA ����
���������������1��ԭ�Ӿ��þ��Ƿ�Ӧ���ԭ��ȫ��ת��Ϊ�����ѡ��ӦI�Ļ��Ϸ�Ӧ����ͼ��֪��T2>T1�������¶ȼ״������ʵ������٣�˵�������¶Ȼ�ѧƽ�����淴Ӧ�����ƶ�������ƽ���ƶ�ԭ���������¶Ȼ�ѧƽ�������ȷ�Ӧ�����ƶ������淴Ӧ���������ȷ�Ӧ����������Ӧ�Ƿ��ȷ�Ӧ���ʡ�H2<0���۷�Ӧ��ʼʱC��CO2��="1mol/L," C(H2)=3mol/L���ڴﵽƽ����c(CO2)= 0��2 mol/L��CO2�ı�Ũ����0��8mol/L,����H2�ı�Ũ��Ϊ2��4mol/L�� H2ƽ��Ũ��Ϊ0��6mol/L�������ļ״���ˮ������Ũ�ȶ���0��8mol/L��ƽ��ʱ��Ũ����2��4mol/L,����ʼʱ��Ũ����4mol/L��������ʱ��ѹǿ�ǿ�ʼ��2��4mol/L��4mol/L=0��6������2����-��+�ۡ�4�ã�2CH3OH(l) + 2O2(g) =" 2CO" (g) + 4H2O(l) ��H =-1275��6 kJ/mol��H =-885��6 kJ/mol�����Բ���1molһ����̼��Һ̬ˮ�ų�������Ϊ442��8 KJ����3���״�ȼ�ϵ�صĸ�����ͨ��״��ĵ缫���缫��ӦΪCH3OH+8OH- -6e- = CO32- +6H2O��ÿĦ���ļ״���Ӧת�Ƶ���9Ħ�������ļ״�1��6��ʱ��n(CH3OH)=1��6g��32g/mol=0��05mol,����ת�Ƶ���0��3 NA�������Դ�ȼ�ϵ��ΪǦ���س�磬��Ӧ��ͼ���Ҳ�缫�������صĸ�����
���㣺����ȼ�ϵ�ء����ص����ڼ��缫��Ӧ������ת�Ƶ�֪ʶ��


 ��ڽ��ȫ������ϵ�д�
��ڽ��ȫ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
I����֪����Ӧ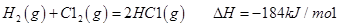
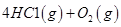
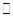
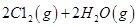

��ش�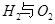 ��Ӧ������̬ˮ���Ȼ�ѧ����ʽ__________________________
��Ӧ������̬ˮ���Ȼ�ѧ����ʽ__________________________
II��ʵʩ�Լ�����Դ�˷Ѻͽ��ͷ����ŷ�Ϊ�������ݵĽ��ܼ������ߣ���Ӧ��ȫ���������⡢������Դ��Լ�͡������Ѻ������ı�Ȼѡ����ҵ�ķ�չ������Ϲ��ҽ��ܼ��ŵ�����Ҫ����������ѧ֪ʶ������������⣺
��1����֪ij��Ӧ��ƽ�����ʽΪ��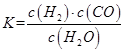
������Ӧ�Ļ�ѧ����ʽΪ��_________________________________________________
��2����֪��400��ʱ����Ӧ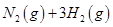
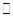
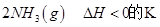 =0��5����400��ʱ����0��5L�ķ�Ӧ�����н��кϳɰ���Ӧ��һ��ʱ����N2��H2��NH3�����ʵ����ֱ�Ϊ2mol��1mol��2mol�����ʱ��Ӧ
=0��5����400��ʱ����0��5L�ķ�Ӧ�����н��кϳɰ���Ӧ��һ��ʱ����N2��H2��NH3�����ʵ����ֱ�Ϊ2mol��1mol��2mol�����ʱ��Ӧ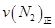 ____________
____________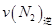 �������������������ȷ������
�������������������ȷ������
��ʹ�ø÷�Ӧ�Ļ�ѧ��Ӧ���ʼӿ죬ͬʱʹƽ��ʱNH3������������ӣ�
�ɲ�ȡ����ȷ��ʩ��____________������ţ�
A���Ӵ��� B�������¶� C����С�������ѹǿ D��ʹ����Һ������
��3����һ��������ܱ������У��������»�ѧ��Ӧ��
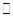
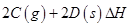 ���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
������������⣺
���жϸ÷�Ӧ��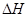 ___________0�������������
___________0�������������
����һ�������£����жϸ÷�Ӧһ���ﻯѧƽ��״̬����___________������ţ���
A�� B��������ѹǿ���ֲ���
B��������ѹǿ���ֲ���
C��A��B��ת������� D�����������ܶȱ��ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ҵ������ʱ�����ô�������Ӧ��SO2ת��ΪSO3��һ���ؼ����衣
��1��ij�¶��£�2SO2��g��+O2��g�� 2SO3��g�� ��H="-197" kj��mol����ʼʱ��10 L���ܱ������м���4��0 mol SO2��g����10��0 mol O2��g��������Ӧ�ﵽƽ��ʱ���ų�197kJ�����������¶��µ�ƽ�ⳣ��K= �������¶�K�� �������С�䡱����
2SO3��g�� ��H="-197" kj��mol����ʼʱ��10 L���ܱ������м���4��0 mol SO2��g����10��0 mol O2��g��������Ӧ�ﵽƽ��ʱ���ų�197kJ�����������¶��µ�ƽ�ⳣ��K= �������¶�K�� �������С�䡱����
��2��һ�������£���һ���������ܱ������г���2mol SO2��1mol O2���������з�Ӧ�� 2SO2��g��+O2��g�� 2SO3��g�����ﵽƽ��ı�����������SO2��O2��SO3��ƽ��Ũ�ȶ���ԭ��������� ������ĸ����
2SO2��g��+O2��g�� 2SO3��g�����ﵽƽ��ı�����������SO2��O2��SO3��ƽ��Ũ�ȶ���ԭ��������� ������ĸ����
A�����º��ݣ�����2mol SO3 B�����º��ݣ�����2mol N2
C�����º�ѹ������1 mol SO3 D�������¶�
��3����һ�ܱ������н������з�Ӧ��2SO2��g��+O2��g��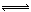 2SO3��g������ѧ��ȤС���ͬѧ̽����������������ʱ���ı�ijһ����ʱ��������Ӧ��Ӱ�죬������ʵ���������������й�ϵͼ�������ж�����ȷ���� ������ĸ����
2SO3��g������ѧ��ȤС���ͬѧ̽����������������ʱ���ı�ijһ����ʱ��������Ӧ��Ӱ�죬������ʵ���������������й�ϵͼ�������ж�����ȷ���� ������ĸ����
A��ͼ���о����Dz�ͬ�����Է�Ӧ��Ӱ�죬����ʹ�õĴ���Ч�ʽϸ�
B��ͼ���о�����ѹǿ�Է�Ӧ��Ӱ�죬�Ҽ�ѹǿ�ϸ�
C��ͼ���о������¶ȶԷ�Ӧ��Ӱ�죬���ҵ��¶Ƚϵ�
D��ͼ���о����Dz�ͬ�����Է�Ӧ��Ӱ�죬�Ҽ�ʹ�õĴ���Ч�ʽϸ�
��4��ijʵ��С����������ͼ��ʾװ���õ绯ѧԭ���������ᣬд��ͨ��SO2�ĵ缫�ĵ缫��Ӧʽ�� ��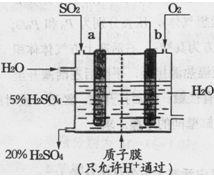
��5�����ղ�����SO2�����������ᡣ��֪25�桢101 kPaʱ��
SO2��g��+O2��g�� 2SO3��g�� ��H1="-197" kJ��mol��
2SO3��g�� ��H1="-197" kJ��mol��
H2O��g��=H2O��1�� ��H2="-44" kJ��mol��
2SO2��g��+O2��g��+2H2O��g��=2H2SO4��1�� H3="-545" kJ��mol��
д��SO3��g����H2O��1����Ӧ���Ȼ�ѧ����ʽ�� ��
��6����������Ƶ������Σ���һ���¶��£���K2SO4��Һ�еμ�Na2CO3��Һ��BaCl2��Һ�������ֳ�������ʱ��SO42-��CO32-��Ũ��֮�� ��[��֪���¶�ʱ��Ksp��BaSO4��=1��3x10-10��KsP��BaCO3��=5��2x10-9]��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
2SO2��g��+ O2��g�� 2SO3��g�� ��H =" a" kJ·mol��1����Ӧ���̵������仯��ͼ��ʾ����֪1mol SO2��g����ȫת��Ϊ1mol SO3��g������99 kJ����ش�
2SO3��g�� ��H =" a" kJ·mol��1����Ӧ���̵������仯��ͼ��ʾ����֪1mol SO2��g����ȫת��Ϊ1mol SO3��g������99 kJ����ش�
��1��ͼ��A���ʾ_______________________��a="__________" ��
��2�� Ea�Ĵ�С�Ը÷�Ӧ�ġ�H _______����С� ���ޡ���Ӱ�졣�÷�Ӧ����V2O5������������V2O5��ʹͼ��B��_________������ߡ��������͡����䡱����
��3����֪������ı�ȼ����Ϊ296kJ·mol��1��д����Ӧ���Ȼ�ѧ����ʽ��________________________ ____�����³�ѹ�£��ɵ������������������Ӧ��������1mol SO3��g�����ų���������Ϊ___ ___ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪H2��g����CO��g����ȼ���ȡ�H�ֱ�Ϊ-285.8kJ��mol-1��-283.0kJ��mol��
��һ����̼��Һ̬ˮ��Ӧ�����ɶ�����̼���������Ȼ�ѧ����ʽΪ
________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���ڴ�������Ϊ��ѧ��ҵ����������ľ���Ч�棬�����о���Ѱ��һֱ���ܵ����ӵĸ߿Ƽ�����
��1��V2O5�ǽӴ���������Ĵ�������ͼΪ��������������2SO2 (g) + O2(g) 2SO3(g) ��H����196.6 kJ��mol��1��Ӧ���̵������仯ʾ��ͼ��
2SO3(g) ��H����196.6 kJ��mol��1��Ӧ���̵������仯ʾ��ͼ��
��V2O5��ʹ�û�ʹͼ��B�� ������ߡ��������͡�����
��һ�������£�SO2�������Ӧtmin��SO2��SO3���ʵ���Ũ�ȷֱ�Ϊa mol/L��b mol/L����SO2��ʼ���ʵ���Ũ��Ϊ mol/L������SO3�Ļ�ѧ��Ӧ����Ϊ mol/(L��min)��
��2����ͼ��һ����ͭ��ϡ����Ϊԭ��������������������ʾ��ͼ��
������CuSO4���ܷ�ӦΪ2Cu+O2+2H2SO4��2 CuSO4+2H2O������ ������ã�ʹ��Ӧ������������ɣ�
������ã�ʹ��Ӧ������������ɣ�
��һ����Cu��2Fe3����2Fe2����Cu2��
�ڶ����� ���������ӷ���ʽ��ʾ��
�ڵ�����ҺpHΪ3��4��Ŀ���� ������ʱ������Լ�����Ϊ ����ѡ����ţ�
a��NaOH��Һ b��CuO��ĩ c��Cu2(OH)2CO3 d����ˮ
��3������TiO2�������Ĺ�����������ҵ�����������Ƶô�TiO2����ת��ΪTiCl4(l)����TiCl4(l)��ȡ����TiO2�ķ���֮һ�ǽ�TiCl4���嵼�����������У�700��1000�棩����ˮ�⡣
��֪��TiO2(s)��2Cl2(g)��TiCl4(l)��O2(g) ��H����140 kJ��mol��1
2C(s)��O2(g)��2CO(g) ��H����221 kJ��mol��1
��д��TiO2�ͽ�̿��������Ӧ����TiCl4��CO���Ȼ�ѧ����ʽ�� ��
��д������TiCl4(l)��ȡ����TiO2�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��1��ij��ѧ��ȤС��Ҫ��ɷ�Ӧ�ȵIJⶨ��ʵ�����ϱ����ձ�����С�����ձ�������ĭ���ϡ���ĭ���ϰ塢��ͷ�ιܡ����β�����������0��50mol�� L��1���ᡢ0��50mol�� L��1NaOH��Һ��ʵ����ȱ�ٵIJ�����Ʒ��_____________��_______________��
��2����֪2molCO������ȫȼ������CO2 ����ų�566 kJ������1 mol������ȫȼ������Һ̬ˮ�ų�286 kJ������1 molCH4������ȫȼ������CO2�����Һ̬ˮ�ų�890 kJ������д���ñ�ȼ������Ϊ��Ӧ�ȵ�COȼ�յ��Ȼ�ѧ����ʽ__________________��
��1 molCH4������ȫȼ������CO2�����Һ̬ˮ���ų�����_____890 kJ�� ������� ����������=����������a molCH4��CO��H2�Ļ��������ȫȼ�գ����� CO2�����Һ̬ˮ����CO2��ˮ�����ʵ������ʱ����ų�������Q���ĵ�ȡֵ��Χ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӳ�Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ����kJ/mol��ʾ��������۲���ͼ��Ȼ��ش����⡣
(l)ͼ����ʾ��Ӧ��______������ȡ����ȡ�����Ӧ���÷�Ӧ_______�����Ҫ������Ҫ�������ȣ��÷�Ӧ�ġ�H=_______���ú� ��
�� �Ĵ���ʽ��ʾ����
�Ĵ���ʽ��ʾ����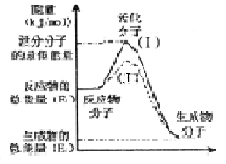
(2)��֪�Ȼ�ѧ����ʽ��H2(g) +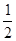 O2(g)�TH2O(g)����H=-241��5kJ/mol���÷�Ӧ�Ļ��Ϊ167�� 4kJ/mol�������淴Ӧ�Ļ��Ϊ________________��
O2(g)�TH2O(g)����H=-241��5kJ/mol���÷�Ӧ�Ļ��Ϊ167�� 4kJ/mol�������淴Ӧ�Ļ��Ϊ________________��
(3)����ͬһ��Ӧ��ͼ������(��)��ʵ��(I)��ȣ���ܴ�ͣ�����ӵİٷ������࣬��Ӧ���ʼӿ죬����Ϊ����ܵ�ԭ����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����P��s����Cl2������Ӧ����PCl3��PCl5����Ӧ���̺�������ϵ��ͼ��ʾ��ͼ�еġ�H��ʾ����1mol��������ݣ�
��ͼ�ش���������
��1��P��Cl2��Ӧ����PCl3���Ȼ�ѧ����ʽ ��
��2��PCl5�ֽ�����PCl3��Cl2���Ȼ�ѧ����ʽ ��
�����ֽⷴ��һ�����淴Ӧ���¶�T1ʱ�����ܱ������м���0.8mol PCl5����Ӧ�ﵽƽ��ʱ��ʣ��0.6mol PCl5����ֽ��ʦ�1���� ������Ӧ�¶���T1���ߵ�T2��ƽ��ʱPCl5�ֽ��ʦ�2����2 ��1������ڡ�����С�ڡ����ڡ�����
��3����ҵ���Ʊ�PCl5ͨ�����������У��Ƚ�P��Cl2��Ӧ�����м����PCl3��Ȼ���£��ٺ�Cl2��Ӧ����PCl5��ԭ���� ��
��4��P��Cl2��������Ӧ����1mol PCl5�ġ�H3= ��P��Cl2һ����Ӧ����1mol PCl5�ġ�H4 ��H3 ������ڡ�����С�ڡ����ڡ�����ԭ���� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com