

 ���������ҹ�ʢ���İ˽������У�����ç�������ʵ�����������˵����ȷ����
���������ҹ�ʢ���İ˽������У�����ç�������ʵ�����������˵����ȷ���� �������к�3��-OH��1��-COOH��1��̼̼˫������ϴ������ᡢϩ�������������
�������к�3��-OH��1��-COOH��1��̼̼˫������ϴ������ᡢϩ�������������


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
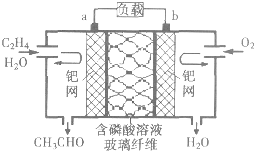 ��ϩ����������ȩ����Ƴ���ͼ��ʾ��ȼ�ϵ�أ������Ʊ���ȩ��ͬʱ��õ��ܣ����ܷ�ӦΪ��2CH2�TCH2+O2��2CH2CHO�������й�˵����ȷ���ǣ�������
��ϩ����������ȩ����Ƴ���ͼ��ʾ��ȼ�ϵ�أ������Ʊ���ȩ��ͬʱ��õ��ܣ����ܷ�ӦΪ��2CH2�TCH2+O2��2CH2CHO�������й�˵����ȷ���ǣ�������| A��������ӦΪ���ȷ�Ӧ |
| B��b��Ϊ�������е�������������������Ӧ |
| C��������ӦʽΪ��CH2�TCH2-2e-+2OH-��CH3CHO+H2O |
| D��ÿ��0.1molO2��Ӧ����Ǩ��H+ 0.4mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c��SO42-����c��HSO3-����c��SO32-����c��H2SO3�� |
| B��c��K+����c��SO32-����c��SO42-����c��HSO3-����c��H+����c��OH-�� |
| C��c��K+���Tc��HSO3-��+2c��SO32-��+2c��SO42-�� |
| D��c��K+��+c��H+���Tc��HSO3-��+c��SO32-��+c��SO42-��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | Na2SO4 |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 7.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ | ���ǰ�ᣨ���Σ���Ũ�� | ��ϱ����������Һ���� |
| A | c��HA��=0.02mol?L-1 | �������ϣ�pH��7 |
| B | HB��Һ��pH=2 | V1 mL NaOH��Һ��V2 mL HB��Һ��pH=7 |
| C | c��H2C��=0.01mol?L-1 | �������ϣ�pH��7 |
| D | c��NaHD��=0.01mol?L-1 | �������ϣ�pH=7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com