
| A. | 舱底镶嵌锌块,锌作负极,以防船体被腐蚀 | |
| B. | 在潮湿的中性环境中,金属的电化学腐蚀主要是析氢腐蚀 | |
| C. | 铁表面镀银,铁作阳极 | |
| D. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
分析 A.作原电池正极的金属被保护;
B.在潮湿的中性环境中,金属的电化学腐蚀主要是吸氧腐蚀;
C.电镀时,镀层作阳极,镀件作阴极;
D.在电解池中,阳极金属易被腐蚀.
解答 解:A.锌、铁和电解质溶液形成原电池时,正极是铁,正极上阳离子得电子发生还原反应,所以铁被保护,故A正确;
B.在潮湿的中性环境中,金属的电化学腐蚀主要是吸氧腐蚀,故B错误;
C.电镀时,镀层作阳极,镀件作阴极,所以铁表面镀银,银作阳极,故C错误;
D.地下输油钢管与外加直流电源的正极相连,在该电解池中,阳极金属铁易被腐蚀,故D错误;
故选A.
点评 本题考查原电池和电解池原理,明确原电池定义、金属腐蚀与防护的方法、电镀原理等知识点即可解答,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 石油裂解得到的汽油是纯净物 | |
| B. | 煤的气化是物理变化 | |
| C. | 天然气是一种清洁的化石燃料 | |
| D. | 水煤气是通过煤的液化得到的气体燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 能发生碱性水解,1 mol该有机物完全反应消耗8 mol NaOH | |
| B. | 常温下,能与Na2CO3溶液反应放出CO2 | |
| C. | 与稀硫酸共热,能生成两种有机物 | |
| D. | 该有机物的分子式为C14H10O9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2 L氧气含有的分子数目为nA | |
| B. | 1 mol H2所含有的电子数目为nA | |
| C. | 4.4 g 二氧化碳含有的分子数目为0.1 nA | |
| D. | 1 mol/L CaCl2溶液中含有的氯离子数目为2nA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
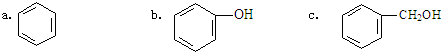
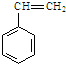 )是一种重要的有机化工原料.
)是一种重要的有机化工原料.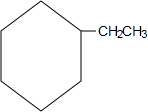 .
.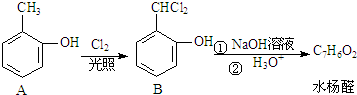
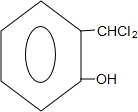 +2NaOH$→_{酸化}^{H_{2}O}$
+2NaOH$→_{酸化}^{H_{2}O}$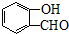 +2NaCl+H2O.
+2NaCl+H2O.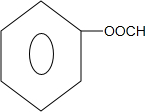 、
、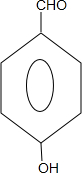 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
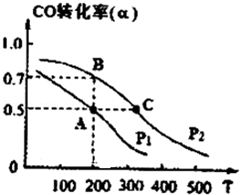 工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2 (g)?CH3OH (g)△H=-116kJ/mol
工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2 (g)?CH3OH (g)△H=-116kJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
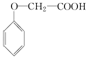 发生化学反应的产物.
发生化学反应的产物.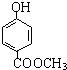 、
、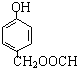 等.
等.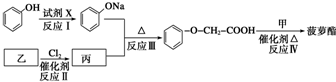
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com