
【题目】常温下,用0.02molL﹣1MOH溶液滴定100mL0.01molL﹣1HA溶液,如图为加入MOH溶液的体积与混合溶液的pH变化情况(溶液体积变化勿略不计).回答下列问题: 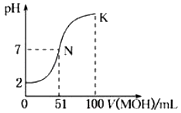
(1)由图中信息可知HA为酸(填“强”或“弱”),滴定所用的最适宜指示剂为 , 滴定时眼睛注视 .
(2)常温下一定浓度的MA稀溶液的pH=a,则a7(填“大于”、“小于”或“等于”)此时,溶液中水电离出的c(OH﹣)=mol/L.
(3)请写出K点所对应的溶液中离子浓度的由大到小的关系: .
(4)K点所对应的溶液中,c(M+)+c(MOH)2c(A﹣);(填“大于”“小于”“等于”)
(5)室温下MOH溶液加水稀释过程中,下列数值变小的是(填序号) ①c(H+) ② ![]() ③c(OH﹣) ④
③c(OH﹣) ④ ![]() .
.
【答案】
(1)强;甲基橙;锥形瓶内颜色变化
(2)<;10﹣a
(3)c(M+)>c(A﹣)>c(OH﹣)>c(H+)
(4)等于
(5)③
【解析】解:(1)根据图知,未加碱时0.01molL﹣1HA溶液的pH=2,说明溶液中c(H+)=c(HA),HA完全电离为强酸; 当混合溶液的pH=7时,n(HA)<n(MOH),说明MOH部分电离为弱碱,二者恰好完全中和时生成的MA是强酸弱碱盐,其溶液呈酸性,所以需要选取甲基橙为指示剂;滴定时眼睛要注视混合溶液颜色变化,所以眼睛要注视锥形瓶内颜色变化,所以答案是:强;甲基橙;锥形瓶内颜色变化;(2)MA是强酸弱碱盐,其阳离子水解导致该溶液呈酸性,所以a<7;水电离出的c(OH﹣)等于该溶液中c(H+)为10﹣a mol/L,所以答案是:<;10﹣a;(3)K点n(MOH)=2n(HA),溶液中的溶质为等物质的量浓度的MOH和MA,MOH电离程度大于MA水解程度导致溶液呈碱性,则c(OH﹣)>c(H+),结合电荷守恒得c(M+)>c(A﹣),MOH电离较微弱,所以溶液中离子浓度大小顺序是c(M+)>c(A﹣)>c(OH﹣)>c(H+),所以答案是:c(M+)>c(A﹣)>c(OH﹣)>c(H+);(4)K点n(MOH)=2n(HA),溶液中存在物料守恒,根据物料守恒得c(M+)+c(MOH)等于2c(A﹣),所以答案是:等于;(5)MOH溶液加水稀释促进MOH电离,但MOH电离增大程度小于溶液体积增大程度,则溶液中c(OH﹣)、c(MOH)、c(M+)都减小,①c(OH﹣)减小,离子积常数不变,则c(H+)增大,故错误;②稀释过程中c(OH﹣)减小, ![]() =
= ![]() 增大,故错误;③稀释过程中促进MOH电离,但其电离增大程度小于溶液体积增大程度,所以c(OH﹣)减小,故正确;④稀释过程中c(OH﹣)、c(M+)减小程度相同,则
增大,故错误;③稀释过程中促进MOH电离,但其电离增大程度小于溶液体积增大程度,所以c(OH﹣)减小,故正确;④稀释过程中c(OH﹣)、c(M+)减小程度相同,则 ![]() 不变,故错误;所以答案是:③.
不变,故错误;所以答案是:③.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)Z(g),经60s达到平衡,生成0.3mol Z,下列说法正确的是( )
A.若增大压强,则物质Y的转化率减小
B.将容器体积变为5 L,Z的平衡浓度变为原来的2倍
C.Y浓度变化表示的反应速率为0.0005 mol/(Ls )
D.若升高温度,X的体积分数增大,则该反应的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质分类说法正确的是( )
A. 纯碱、液态氧、碘酒、稀盐酸依次是盐、单质、混合物、电解质
B. 干冰、生石灰、硫酸、碳酸氢铵依次是单质、氧化物、酸、盐
C. 氯化氢、氨气、水银、草木灰依次是电解质、非电解质、单质、混合物
D. 冰水、空气、泥水依次是溶液、胶体、浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是( )
A. 图表示25℃时,用0.1 molL﹣1盐酸滴定20 mL 0.1 molL﹣1 NaOH溶液,溶液的pH随加入酸体积的变化
图表示25℃时,用0.1 molL﹣1盐酸滴定20 mL 0.1 molL﹣1 NaOH溶液,溶液的pH随加入酸体积的变化
B.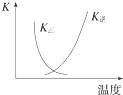 图中曲线表示反应2SO2(g)+O2(g)2SO3(g)△H<0正、逆反应的平衡常数K随温度的变化
图中曲线表示反应2SO2(g)+O2(g)2SO3(g)△H<0正、逆反应的平衡常数K随温度的变化
C. 图表示10 mL 0.01 molL﹣1 KMnO4酸性溶液与过量的0.1 molL﹣1 H2C2O4溶液混合时,n(Mn2+)随时间的变化
图表示10 mL 0.01 molL﹣1 KMnO4酸性溶液与过量的0.1 molL﹣1 H2C2O4溶液混合时,n(Mn2+)随时间的变化
D.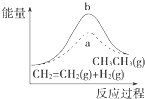 图中a、b曲线分别表示反应CH2═CH2(g)+H2(g)﹣→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的能量变化
图中a、b曲线分别表示反应CH2═CH2(g)+H2(g)﹣→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
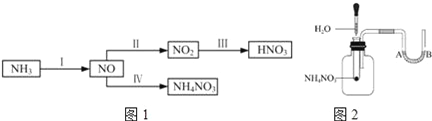
【题目】NH3经一系列反应可以得到HNO3和NH4NO3,如图1所示.
【资料卡片】
i.NH4NO3是一种白色晶体,易溶于水,微溶于乙醇.
ii.在230℃以上时,同时有弱光:2NH4NO3═2N2↑+O2↑+4H2O
iii.在400℃以上时,剧烈分解发生爆炸:4NH4NO3═3N2↑+2NO2+8↑H2O
(1)如图2将水滴入盛有硝酸铵的试管中,观察到的A处液面上升,B处液面下降,产生该现象的原因________.一段时间后还能观察到的现象是____________.
(2)实验室可以用氯化铵和熟石灰反应来制备氨气,该反应的化学方程式是______,能否用硝酸铵代替氯化铵,______(填“能”或“不能”),理由是______.
(3)从反应类型角度分析在I~IV的转化过程中的共同点是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com